Výběr vhodných technologií pro oddělování v farmaceutickém průmyslu je rozhodující krok, který přímo ovlivňuje kvalitu výrobku, dodržení předpisů a provozní efektivitu v farmaceutickém výrobě. Tato volba vyžaduje posouzení několika faktorů, včetně konkrétních sloučenin, které se zpracovávají, požadované úrovně čistoty, objemů výroby a předpisů, které upravují farmaceutické výrobní procesy.

Farmaceutický průmysl spoléhá na přesné metody separace, aby zajistil, že účinné farmaceutické látky splňují přísné požadavky na kvalitu, a zároveň zachovává cenovou efektivnost a škálovatelnost. Pochopení rozhodovacího rámce pro farmaceutické technologie separace umožňuje výrobcům optimalizovat své procesy, snižovat rizika kontaminace a dosahovat konzistentních specifikací výrobků, které splňují jak požadavky regulačních schválení, tak komerční životaschopnosti.
Pochopení kategorií farmaceutických technologií separace
Strojní technologie separace
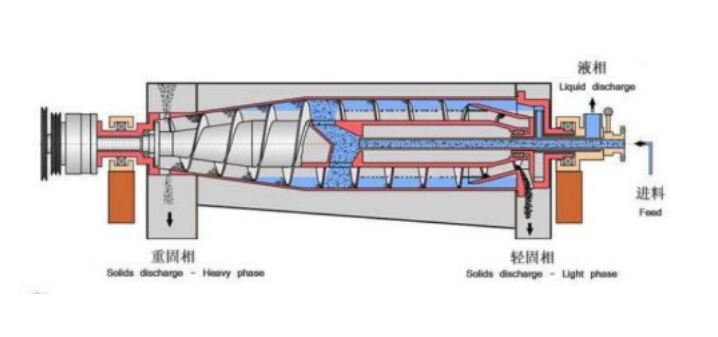
Mechanické farmaceutické technologie separace využívají fyzikální síly k oddělení částic na základě rozdílů v jejich velikosti, hustotě nebo tvaru. Tyto metody zahrnují centrifugaci, filtrace a síťování, které probíhají bez chemických reakcí nebo změn fáze. Centrifugální separátory, zejména odstředivé odstředivky typu decanter, se vynikajícím způsobem hodí k oddělování pevných částic od kapalné fáze ve farmaceutické výrobě.
Výběr mechanických technologií oddělování v farmaceutickém průmyslu závisí na rozdělení velikosti částic, rozdílech hustot mezi fázemi a požadované účinnosti oddělování. Tyto systémy nabízejí výhody spojené s nepřetržitým provozem, škálovatelností a minimálním chemickým kontaminováním, čímž se stávají vhodnými pro zpracování farmaceutických meziproduktů a konečných produktů, kde je klíčové zachování chemické integrity.
Mechanické metody oddělování poskytují také vynikající kontrolu provozních parametrů, jako je odstředivá síla (G-síla), doba pobytu a průtokové rychlosti. Tato kontrola umožňuje farmaceutickým výrobcům optimalizovat výkon oddělování při zachování konzistentní kvality výrobku a splnění regulačních požadavků na zařízení používaná ve farmaceutickém zpracování.
Chemické a chromatografické metody oddělování
Chemické metody oddělování v farmaceutických separačních technologiích zahrnují selektivní rozpouštění, srážení nebo extrakci, které využívají rozdíly v chemických vlastnostech mezi cílovými sloučeninami a nečistotami. Tyto metody často poskytují vyšší selektivitu než mechanické metody, avšak vyžadují pečlivé zvážení chemické kompatibility a požadavků na následné zpracování.
Chromatografické farmaceutické separační technologie nabízejí výjimečnou přesnost při čištění účinných farmaceutických látek a odstraňování blízce příbuzných nečistot. Tyto systémy využívají stacionární a mobilní fázi k dosažení selektivního oddělení na základě molekulárních interakcí, avšak obvykle pracují v dávkovém režimu a vyžadují specializovanou odbornou způsobilost pro optimalizaci a údržbu.
Volba mezi chemickými a chromatografickými metodami závisí na požadované úrovni čistoty, rozsahu provozu a ekonomických ohledů. Ačkoli tyto farmaceutické separační technologie dokážou dosáhnout velmi vysoké selektivity, často spojují vyšší provozní náklady a složitější řízení procesu ve srovnání s mechanickými separačními přístupy.
Hodnocení požadavků a specifikací procesu
Standardy kvality a čistoty výrobku
Farmaceutické separační technologie je třeba vybírat na základě konkrétních požadavků na čistotu stanovených farmakopejními normami a regulačními orgány. Požadovaná úroveň čistoty přímo ovlivňuje složitost a náklady separačního systému, přičemž vyšší požadavky na čistotu obvykle vyžadují více separačních stupňů nebo sofistikovanější technologie.
Pochopení povahy a koncentrace nečistot přítomných ve vstupním materiálu je zásadní pro výběr vhodných farmaceutických separačních technologií. Některé nečistoty mohou vyžadovat specifické separační mechanismy, zatímco jiné lze účinně odstranit pomocí univerzálního separačního zařízení, jako jsou například vysokovýkonné odstředivky nebo pokročilé filtrační systémy.
Při výběru farmaceutických separačních technologií je třeba také zohlednit analytické metody používané ke kontrole výkonu separace. Zvolený separační systém by měl produkovat látky, které lze snadno analyzovat pomocí běžných farmaceutických zkušebních metod a zároveň splňovat stanovené specifikace týkající se identifikace, čistoty a účinnosti.
Velikost výrobního měřítka a požadavky na výkon
Požadavky na objem výroby výrazně ovlivňují výběr farmaceutických separačních technologií, protože různé technologie vykazují odlišné charakteristiky škálovatelnosti a propustnosti. Malé laboratorní separace mohou využívat jiné přístupy než velkoobjemová komerční výroba, což vyžaduje pečlivé zvážení možností zvětšení měřítka.
Preference spojitého versus dávkového provozu také ovlivňují výběr farmaceutických separačních technologií. Spojité separační systémy, jako jsou farmaceutické technologie separace s použitím odstředivek typu decanter nabízejí výhody pro výrobu ve velkém množství, zatímco dávkové systémy mohou poskytnout lepší řízení u specializovaných nebo vysoce hodnotných produktů.
Při výběru farmaceutických separačních technologií je třeba posoudit pružnost systémů při zpracování různých složení přívodních směsí a výrobních plánů. Systémy, které dokážou přizpůsobit svůj provoz změnám ve vlastnostech přívodních směsí nebo výrobním požadavkům, nabízejí provozní výhody a přispívají k optimalizaci celkové výrobní účinnosti.
Regulační a dodržovací aspekty
Požadavky na dobré výrobní postupy
Všechny farmaceutické separační technologie musí splňovat požadavky na správnou výrobní praxi (GMP), které upravují konstrukci zařízení, jeho provoz a údržbu ve farmaceutických výrobních zařízeních. Tyto požadavky zahrnují specifikace materiálů použitých pro výrobu zařízení, povrchové úpravy, postupy čištění a dokumentační systémy, které zajišťují kvalitu výrobku a bezpečnost pacientů.
Požadavky na validaci technologií oddělování v farmaceutickém průmyslu zahrnují komplexní testování a dokumentaci, které prokazují, že zařízení konzistentně vyrábí výrobky splňující předem stanovené specifikace. Tento proces zahrnuje fáze kvalifikace instalace, kvalifikace provozu a kvalifikace výkonu, které musí být dokončeny před zahájením komerčního provozu.
Pro farmaceutické technologie oddělování je nutné zavést postupy řízení změn, aby byly správně řízeny úpravy provozních parametrů, údržbových postupů nebo konfigurací zařízení. Tyto postupy zajistí, že jakékoli změny budou řádně vyhodnoceny, schváleny a zdokumentovány, čímž se udrží soulad s předpisy a zaručí se kvalita výrobku.
Standardy dokumentace a stopovatelnosti
Farmaceutické technologie pro separaci vyžadují komplexní systémy dokumentace, které sledují výkon zařízení, údržbové aktivity a provozní parametry po celou dobu životního cyklu výrobku. Tyto záznamy je nutné vést v souladu s předpisy a mít je k dispozici pro kontrolu regulačními orgány.
Požadavky na sledovatelnost u farmaceutických technologií pro separaci zahrnují vedení podrobných záznamů o vstupních materiálech, provozních podmínkách a výstupních produktech pro každou výrobní šarži. Tato informace umožňuje rychlé vyšetření problémů s kvalitou a podporuje postupy stažení výrobku z trhu v případě nutnosti.
Elektronické systémy záznamů používané u farmaceutických technologií pro separaci musí splňovat předpisy týkající se integritu dat, včetně ustanovení pro zabezpečené ukládání, řízený přístup a auditní stopy, které sledují všechny změny nebo odstranění dat v průběhu času.
Ekonomické a provozní faktory
Kapitálové investice a provozní náklady
Celkové náklady na vlastnictví technologií oddělování v farmaceutickém průmyslu zahrnují pořizovací cenu za zařízení, náklady na instalaci, průběžné náklady na údržbu a spotřebu užitkových služeb během celého životního cyklu zařízení. Tyto náklady je nutné vyhodnotit ve vztahu k očekávaným objemům výroby a maržím z produktů, aby byla určena ekonomická životaschopnost.
Provozní náklady na farmaceutické separační technologie zahrnují spotřební materiál, spotřebu energie, personální náklady a náklady na likvidaci odpadů. Energeticky účinné separační systémy mohou během životnosti zařízení přinést významné úspory, zejména u provozů s vysokým výkonem, kde náklady na užitkové služby tvoří významnou část provozních nákladů.
Náklady na údržbu technologií pro oddělování v farmaceutickém průmyslu se výrazně liší v závislosti na složitosti zařízení, provozním prostředí a požadavcích na údržbu. Jednoduché mechanické separační systémy obvykle vykazují nižší náklady na údržbu ve srovnání se složitějšími chromatografickými nebo chemickými separačními systémy, které vyžadují specializovanou technickou podporu a náhradní komponenty.
Životní cyklus technologie a riziko zastarání
Očekávaná životnost farmaceutických separačních technologií by měla být posouzena ve vztahu k předpokládanému životnímu cyklu výrobku a regulačnímu prostředí. Technologie s dlouhou životností a ověřenou podporou dodavatelů poskytují vyšší dlouhodobou hodnotu a snižují riziko zastarání v průběhu kritických výrobních období.
Stabilita dodavatelů a dostupnost technické podpory jsou klíčové faktory při výběru farmaceutických separačních technologií, protože výrobci zařízení musí poskytovat průběžnou podporu pro náhradní díly, technickou pomoc a aktualizace týkající se dodržování předpisů po celou dobu životního cyklu zařízení.
Při zavádění farmaceutických separačních technologií je třeba zohlednit možnosti technologického vylepšení, aby bylo zařízení možné upravit nebo rozšířit v souladu s měnícími se požadavky výroby nebo s novými předpisy, aniž by bylo nutné zařízení zcela nahradit.
Strategie implementace a optimalizace
Integrace do stávajících výrobních systémů
Úspěšné zavedení farmaceutických separačních technologií vyžaduje pečlivou integraci do stávající výrobní infrastruktury, včetně procesů před a po separaci, systémů užitkových služeb a řídicích systémů. Tato integrace zajišťuje hladký tok materiálu a optimální celkovou účinnost procesu při zachování požadovaných standardů kvality výrobku.
Kompatibilita řídicího systému je zásadní při integraci farmaceutických separačních technologií se stávajícím výrobním zařízením. Moderní separační systémy by měly poskytovat standardizované komunikační protokoly a datová rozhraní, která umožňují bezproblémovou integraci se řídicími a monitorovacími systémy celé výrobní haly.
Požadavky na školení obsluhy farmaceutických separačních technologií je nutné vyhodnotit, aby byla zajištěna dostatečná odborná způsobilost pro bezpečný a účinný provoz zařízení. Školicí programy by měly zahrnovat běžný provoz, odstraňování poruch, postupy údržby a protokoly pro reakci na mimořádné události specifické pro vybranou separační technologii.
Sledování a optimalizace výkonu
Systémy nepřetržitého monitorování pro farmaceutické separační technologie umožňují reálné hodnocení výkonu separace a včasnou detekci potenciálních problémů, které by mohly ovlivnit kvalitu výrobku. Tyto systémy by měly sledovat klíčové ukazatele výkonu, jako je účinnost separace, průtokové rychlosti a parametry kvality výrobku.
Optimalizace procesů pro farmaceutické separační technologie zahrnuje systematické hodnocení provozních parametrů za účelem maximalizace separačního výkonu při současném minimalizování provozních nákladů a zachování souladu s předpisy.
Pravidelné revize výkonu farmaceutických separačních technologií pomáhají identifikovat příležitosti ke zlepšení a zajistit trvalý soulad s vyvíjejícími se předpisovými požadavky. Tyto revize by měly zahrnovat analýzu dat o procesu, záznamů o údržbě a trendů kvality výrobku, aby podporovaly iniciativy pro nepřetržité zlepšování.
Často kladené otázky
Jaké jsou nejdůležitější faktory při výběru farmaceutických separačních technologií?
Mezi nejdůležitější faktory patří požadavky na soulad s předpisy, specifikace čistoty výrobku, měřítko výroby a celkové náklady na vlastnictví. Vybraná technologie musí splňovat standardy dobré výrobní praxe (GMP) a zároveň dosahovat požadované účinnosti oddělování a zachovávat ekonomickou životaschopnost pro zamýšlené objemy výroby.
Jak ovlivňují předpisové požadavky výběr farmaceutických separačních technologií?
Předpisové požadavky stanovují, že farmaceutické separační technologie musí být v souladu s pokyny pro dobrou výrobní praxi (GMP), včetně validace zařízení, systémů dokumentace a postupů řízení změn. Tyto požadavky často upřednostňují osvědčené technologie s prokázaným předpisovým uznáním a komplexní podporou dodavatelů při aktivitách souvisejících s validací.
Jaká je typická doba trvání validace při zavádění nových farmaceutických separačních technologií?
Časové rámce pro validaci technologií oddělování v farmaceutickém průmyslu se obvykle pohybují od 6 do 18 měsíců, a to v závislosti na složitosti zařízení a regulačních požadavcích. Tento časový rámec zahrnuje fáze kvalifikace instalace, kvalifikace provozu, kvalifikace výkonu a validace procesu, které je třeba dokončit před zahájením komerční výroby.
Jak posuzujete dlouhodobou životaschopnost technologií oddělování v farmacii?
Posouzení dlouhodobé životaschopnosti zohledňuje zralost technologie, stabilitu dodavatele, požadavky na údržbu a regulační přijetí. Technologie s ověřeným provozním záznamem, spolehlivou podporou dodavatele a kompatibilitou s nově vznikajícími regulačními trendy poskytují vyšší dlouhodobou hodnotu a snižují riziko zastarání pro farmaceutické výrobní provozy.
Obsah
- Pochopení kategorií farmaceutických technologií separace
- Hodnocení požadavků a specifikací procesu
- Regulační a dodržovací aspekty
- Ekonomické a provozní faktory
- Strategie implementace a optimalizace
-
Často kladené otázky
- Jaké jsou nejdůležitější faktory při výběru farmaceutických separačních technologií?
- Jak ovlivňují předpisové požadavky výběr farmaceutických separačních technologií?
- Jaká je typická doba trvání validace při zavádění nových farmaceutických separačních technologií?
- Jak posuzujete dlouhodobou životaschopnost technologií oddělování v farmacii?