Het selecteren van de juiste farmaceutische scheidingsmethoden is een cruciale beslissing die direct van invloed is op productkwaliteit, naleving van regelgeving en operationele efficiëntie in de farmaceutische productie. De keuze vereist het beoordelen van meerdere factoren, waaronder de specifieke stoffen die worden verwerkt, de vereiste zuiverheidsniveaus, de productievolumes en de regelgeving die van toepassing is op farmaceutische productieprocessen.

De farmaceutische industrie is aangewezen op nauwkeurige scheidingsmethoden om ervoor te zorgen dat werkzame farmaceutische bestanddelen voldoen aan strenge kwaliteitsnormen, terwijl tegelijkertijd kostenefficiëntie en schaalbaarheid worden behouden. Een goed begrip van het beslissingskader voor farmaceutische scheidingsmethoden stelt producenten in staat hun processen te optimaliseren, risico’s op besmetting te verminderen en consistente producteigenschappen te bereiken die voldoen aan zowel regelgevende goedkeuring als commerciële haalbaarheid.
Inzicht in categorieën van farmaceutische scheidingsmethoden
Mechanische Scheidingstechnologieën
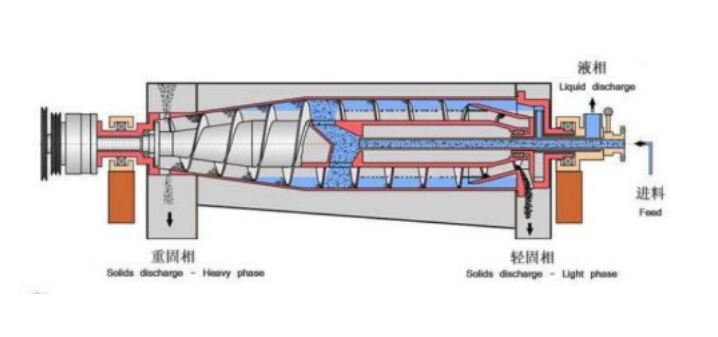
Mechanische farmaceutische scheidingsmethoden maken gebruik van fysieke krachten om deeltjes te scheiden op basis van verschillen in grootte, dichtheid of vorm. Deze methoden omvatten centrifugatie, filtratie en zeefprocessen die werken zonder chemische reacties of fasewisselingen. Centrifugale scheidingsapparaten, met name decantercentrifuges, zijn bijzonder geschikt voor het scheiden van vaste deeltjes uit vloeibare fasen in de farmaceutische productie.
De keuze van mechanische farmaceutische scheidingsmethoden hangt af van de verdeling van de deeltjesgrootte, de dichtheidsverschillen tussen de fasen en de vereiste scheidingsrendement. Deze systemen bieden voordelen op het gebied van continu bedrijf, schaalbaarheid en minimale chemische besmetting, waardoor ze geschikt zijn voor de verwerking van farmaceutische tussenproducten en eindproducten waarbij het behoud van chemische integriteit van essentieel belang is.
Mechanische scheidingsmethoden bieden ook uitstekende controle over bedrijfsparameters zoals G-kracht, verblijftijd en doorvoersnelheden. Deze controle stelt farmaceutische fabrikanten in staat de scheidingsprestaties te optimaliseren, terwijl ze een consistente productkwaliteit behouden en voldoen aan de wettelijke vereisten voor farmaceutische procesapparatuur.
Chemische en chromatografische scheidingsmethoden
Chemische scheidingsaanpakken binnen farmaceutische scheidingsmethoden omvatten selectieve oplossing, neerslagvorming of extractieprocessen die gebruikmaken van chemische eigenschapsverschillen tussen doelverbindingen en verontreinigingen. Deze methoden bieden vaak een hogere selectiviteit dan mechanische aanpakken, maar vereisen zorgvuldige afweging van chemische verenigbaarheid en downstream-verwerkingsvereisten.
Chromatografische farmaceutische scheidingsmethoden bieden uitzonderlijke precisie voor het zuiveren van werkzame farmaceutische bestanddelen en het verwijderen van nauw verwante verontreinigingen. Deze systemen maken gebruik van stationaire en mobiele fasen om selectieve scheiding te bereiken op basis van moleculaire interacties, hoewel ze meestal in batchmodus werken en gespecialiseerde expertise vereisen voor optimalisatie en onderhoud.
De keuze tussen chemische en chromatografische methoden hangt af van de vereiste zuiverheidsniveaus, de schaal van de operatie en economische overwegingen. Hoewel deze farmaceutische scheidingsmethoden zeer hoge selectiviteit kunnen bereiken, brengen ze vaak hogere bedrijfskosten met zich mee en vereisen ze een complexere procesregeling dan mechanische scheidingsmethoden.
Beoordelen van procesvereisten en specificaties
Productkwaliteit en zuiverheidsnormen
Farmaceutische scheidingsmethoden moeten worden geselecteerd op basis van de specifieke zuiverheidseisen die zijn vastgesteld door farmacopeeën en regelgevende instanties. Het gewenste zuiverheidsniveau beïnvloedt direct de complexiteit en de kosten van het scheidingsysteem, waarbij hogere zuiverheidseisen doorgaans meerdere scheidingsstappen of geavanceerdere technologieën vereisen.
Het begrijpen van de aard en concentratie van verontreinigingen in het uitgangsmateriaal is essentieel voor de keuze van geschikte farmaceutische scheidingsmethoden. Sommige verontreinigingen vereisen specifieke scheidingsmechanismen, terwijl andere effectief kunnen worden verwijderd met algemene scheidingsapparatuur, zoals hoogwaardige centrifuges of geavanceerde filtersystemen.
De analytische methoden die worden gebruikt om de scheidingsprestaties te verifiëren, moeten eveneens in overweging worden genomen bij de keuze van farmaceutische scheidingsmethoden. Het gekozen scheidingsysteem dient producten te leveren die gemakkelijk kunnen worden geanalyseerd met behulp van standaard farmaceutische testmethoden, terwijl zij tegelijkertijd voldoen aan de vastgestelde specificaties voor identiteit, zuiverheid en potentie.
Productieschaal en doorvoervereisten
De vereisten voor productievolume beïnvloeden aanzienlijk de keuze van farmaceutische scheidingsmethoden, aangezien verschillende technologieën uiteenlopende schaalbaarheidskenmerken en doorvoervermogens vertonen. Kleinschalige laboratoriumscheidingen kunnen gebruikmaken van andere benaderingen dan grootschalige commerciële productie, wat zorgvuldige overweging van de haalbaarheid van opschaling vereist.
Voorkeuren voor continue of batchverwerking hebben eveneens invloed op de keuze van farmaceutische scheidingsmethoden. Continue scheidingsystemen, zoals farmaceutische scheidingstechnologieën met behulp van decantercentrifuges bieden voordelen voor productie in grote volumes, terwijl batchsystemen mogelijk betere controle bieden voor speciale of hoogwaardige producten.
De flexibiliteit om wisselende voedingssamenstellingen en productieschema’s te verwerken, dient te worden beoordeeld bij de keuze van farmaceutische scheidingsmethoden. Systemen die aanpassingen in voedingskenmerken of productiebehoeften kunnen opvangen, bieden operationele voordelen en dragen bij aan de optimalisatie van de algehele productie-efficiëntie.
Wettelijke en nalevingsoverwegingen
Eisen volgens de goede productiepraktijk
Alle farmaceutische scheidingsmethoden moeten voldoen aan de richtlijnen voor Goede Vervaardigingspraktijk (GVP), die van toepassing zijn op het ontwerp, de bediening en het onderhoud van apparatuur in farmaceutische productiefaciliteiten. Deze eisen omvatten specificaties voor constructiematerialen, oppervlakteafwerkingen, reinigingsprocedures en documentatiesystemen die kwaliteit van het product en veiligheid van de patiënt waarborgen.
De validatievereisten voor farmaceutische scheidingsmethoden omvatten uitgebreide tests en documentatie om aan te tonen dat de apparatuur consistent producten produceert die voldoen aan vooraf bepaalde specificaties. Dit proces omvat de fasen installatiekwalificatie, bedrijfskwalificatie en prestatiekwalificatie, die moeten zijn voltooid voordat commerciële exploitatie kan beginnen.
Er moeten wijzigingsbeheerprocedures worden opgesteld voor farmaceutische scheidingsmethoden om wijzigingen in bedrijfsparameters, onderhoudsprocedures of apparatuurconfiguraties te beheren. Deze procedures waarborgen dat alle wijzigingen adequaat worden geëvalueerd, goedgekeurd en gedocumenteerd om naleving van regelgeving en productkwaliteit te behouden.
Documentatie- en Traceerbaarheidsnormen
Farmaceutische scheidingsmethoden vereisen uitgebreide documentatiesystemen die de prestaties van apparatuur, onderhoudsactiviteiten en procesparameters tijdens de gehele levenscyclus van het product bijhouden. Deze registraties moeten worden bijgehouden conform de wettelijke en regelgevende eisen en moeten op verzoek beschikbaar zijn voor inspectie door de toezichthoudende autoriteiten.
De traceerbaarheidseisen voor farmaceutische scheidingsmethoden omvatten het bijhouden van gedetailleerde registraties van uitgangsmaterialen, verwerkingsomstandigheden en productuitvoer voor elke productiebatch. Deze informatie maakt een snelle onderzoek naar kwaliteitsproblemen mogelijk en ondersteunt, indien nodig, procedures voor productterugroep.
Elektronische registratiesystemen die worden gebruikt in combinatie met farmaceutische scheidingsmethoden moeten voldoen aan de wettelijke en regelgevende eisen voor gegevensintegriteit, inclusief bepalingen voor veilige opslag, gecontroleerde toegang en audittrails die alle wijzigingen of verwijderingen van gegevens in de tijd bijhouden.
Economische en operationele factoren
Capaciteitsinvesteringen en Bedrijfskosten
De totale eigendomskosten voor farmaceutische scheidingsmethoden omvatten de initiële aanschaf van apparatuur, installatiekosten, voortdurende onderhoudskosten en het energieverbruik gedurende de levenscyclus van de apparatuur. Deze kosten moeten worden afgewogen tegen de verwachte productievolume en productmarges om de economische haalbaarheid te bepalen.
De bedrijfskosten voor farmaceutische scheidingsmethoden omvatten verbruiksartikelen, energieverbruik, personeelsbehoeften en kosten voor afvalverwijdering. Energie-efficiënte scheidingsystemen kunnen aanzienlijke kostenbesparingen opleveren gedurende de levensduur van de apparatuur, met name bij hoogwaardige operaties waarbij de nutsvoorzieningskosten een aanzienlijk deel van de bedrijfskosten vertegenwoordigen.
Onderhoudskosten voor farmaceutische scheidingsmethoden variëren sterk op basis van de complexiteit van de apparatuur, de bedrijfsomgeving en de onderhoudseisen. Eenvoudige mechanische scheidingsystemen bieden doorgaans lagere onderhoudskosten dan complexe chromatografische of chemische scheidingsystemen die gespecialiseerde technische ondersteuning en vervangende onderdelen vereisen.
Technologielevenscyclus en obsolescentierisico
De verwachte levensduur van farmaceutische scheidingsmethoden dient te worden beoordeeld in relatie tot de verwachte productlevenscyclus en het regelgevingskader. Technologieën met een lange levensduur en een gevestigde leveranciersondersteuning bieden meer langetermijnwaarde en verminderen het risico op obsolescentie tijdens kritieke productieperiodes.
Leveranciersstabiliteit en de beschikbaarheid van technische ondersteuning zijn cruciale factoren bij de keuze van farmaceutische scheidingsmethoden, aangezien fabrikanten van apparatuur continue ondersteuning moeten bieden voor reserveonderdelen, technische assistentie en updates met betrekking tot naleving van regelgeving gedurende de gehele levenscyclus van de apparatuur.
Bij de implementatie van farmaceutische scheidingsmethoden dient rekening te worden gehouden met mogelijke technologische upgrades, zodat de apparatuur kan worden aangepast of verbeterd naarmate de productievereisten veranderen of nieuwe regelgeving wordt ingevoerd, zonder dat een volledige vervanging nodig is.
Implementatie- en Optimalisatiestrategieën
Integratie met bestaande productiesystemen
Een succesvolle implementatie van farmaceutische scheidingsmethoden vereist een zorgvuldige integratie met de bestaande productie-infrastructuur, inclusief upstream- en downstreamprocessen, nutsvoorzieningssystemen en besturingssystemen. Deze integratie waarborgt een vlotte materiaalstroming en optimale algehele procesefficiëntie, terwijl de kwaliteitsnormen voor het product worden gehandhaafd.
Compatibiliteit van het controlesysteem is essentieel bij de integratie van farmaceutische scheidingsprocessen met bestaande productieapparatuur. Moderne scheidingsystemen moeten gestandaardiseerde communicatieprotocollen en gegevensinterfaces bieden die naadloze integratie met bedrijfsbrede controle- en bewakingssystemen mogelijk maken.
De opleidingsvereisten voor operators van farmaceutische scheidingsprocessen moeten worden beoordeeld om te waarborgen dat voldoende expertise beschikbaar is voor een veilige en effectieve bediening van de apparatuur. Opleidingsprogramma's moeten normale bediening, probleemoplossing, onderhoudsprocedures en noodresponsprotocollen omvatten die specifiek zijn voor de gekozen scheidingsmethode.
Prestatiebewaking en Optimalisatie
Continue bewakingssystemen voor farmaceutische scheidingsprocessen maken real-time beoordeling van de scheidingsprestaties en vroegtijdige detectie van mogelijke problemen mogelijk die van invloed kunnen zijn op de productkwaliteit. Deze systemen moeten belangrijke prestatie-indicatoren volgen, zoals scheidingsrendement, doorvoersnelheden en parameters voor productkwaliteit.
Procesoptimalisatie voor farmaceutische scheidingsmethoden omvat een systematische evaluatie van bedrijfsparameters om de scheidingsprestaties te maximaliseren, tegelijkertijd de bedrijfskosten te minimaliseren en naleving van regelgeving te waarborgen. Deze optimalisatie moet gebaseerd zijn op statistisch ontworpen experimenten en gevalideerde analytische methoden.
Regelmatige prestatiebeoordelingen van farmaceutische scheidingsmethoden helpen verbetermogelijkheden te identificeren en zorgen voor voortdurende naleving van zich ontwikkelende regelgevingseisen. Deze beoordelingen moeten onder andere een analyse omvatten van procesgegevens, onderhoudsregistraties en productkwaliteitstrends ter ondersteuning van initiatieven voor continue verbetering.
Veelgestelde vragen
Wat zijn de meest kritieke factoren bij het kiezen van farmaceutische scheidingsmethoden?
De meest kritieke factoren omvatten vereisten voor naleving van regelgeving, specificaties voor productzuiverheid, productieschaal en totale eigendomskosten. De geselecteerde technologie moet voldoen aan de richtlijnen voor Goede Vervaardigingspraktijk (GVP), terwijl tegelijkertijd de vereiste scheidingsrendementen worden behaald en de economische levensvatbaarheid voor de beoogde productievolume wordt gewaarborgd.
Hoe beïnvloeden regelgevende vereisten de keuze van farmaceutische scheidingsmethoden?
Regelgevende vereisten stellen dat farmaceutische scheidingsmethoden moeten voldoen aan de richtlijnen voor Goede Vervaardigingspraktijk (GVP), inclusief validatie van apparatuur, documentatiesystemen en procedures voor wijzigingsbeheer. Deze vereisten geven vaak de voorkeur aan gevestigde technologieën met een bewezen regelgevende acceptatie en uitgebreide ondersteuning door leveranciers bij validatieactiviteiten.
Wat is de typische validatietijdsduur voor de implementatie van nieuwe farmaceutische scheidingsmethoden?
De validatietijdschema's voor farmaceutische scheidingsmethoden liggen doorgaans tussen de 6 en 18 maanden, afhankelijk van de complexiteit van de apparatuur en de regelgevende vereisten. Dit tijdschema omvat de fasen installatiekwalificatie, bedrijfskwalificatie, prestatiekwalificatie en procesvalidatie, die allemaal moeten zijn voltooid voordat commerciële productie kan beginnen.
Hoe beoordeelt u de langetermijnlevensvatbaarheid van farmaceutische scheidingsmethoden?
Bij de beoordeling van de langetermijnlevensvatbaarheid worden technologiematuriteit, stabiliteit van leveranciers, onderhoudseisen en regelgevende acceptatie in overweging genomen. Technologieën met een bewezen geschiedenis, betrouwbare ondersteuning door leveranciers en compatibiliteit met opkomende regelgevende trends bieden meer langetermijnwaarde en verminderen het risico op veroudering voor farmaceutische productieprocessen.
Inhoudsopgave
- Inzicht in categorieën van farmaceutische scheidingsmethoden
- Beoordelen van procesvereisten en specificaties
- Wettelijke en nalevingsoverwegingen
- Economische en operationele factoren
- Implementatie- en Optimalisatiestrategieën
-
Veelgestelde vragen
- Wat zijn de meest kritieke factoren bij het kiezen van farmaceutische scheidingsmethoden?
- Hoe beïnvloeden regelgevende vereisten de keuze van farmaceutische scheidingsmethoden?
- Wat is de typische validatietijdsduur voor de implementatie van nieuwe farmaceutische scheidingsmethoden?
- Hoe beoordeelt u de langetermijnlevensvatbaarheid van farmaceutische scheidingsmethoden?