適切な医薬品分離技術を選定することは、製品品質、規制対応性、および医薬品製造における運用効率に直接影響を与える極めて重要な判断です。この選定には、処理対象となる特定の化合物、求められる純度レベル、生産量、および医薬品製造工程を規制する要件など、複数の要素を評価する必要があります。

製薬業界では、有効成分が厳格な品質基準を満たすことを保証するとともに、コスト効率性およびスケーラビリティを維持するために、正確な分離手法に依存しています。製薬分離技術に関する意思決定フレームワークを理解することで、メーカーは自社のプロセスを最適化し、汚染リスクを低減し、規制承認および商業的実現可能性の両方の要件を満たす一貫した製品仕様を達成できます。
製薬分離技術のカテゴリーの理解
機械的分離技術
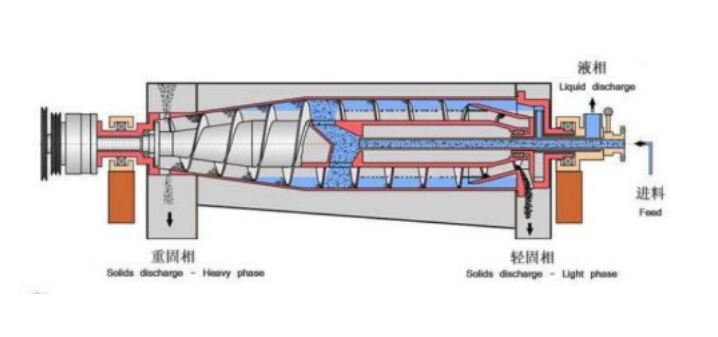
機械式製薬分離技術は、粒子のサイズ、密度、または形状の差異に基づいて物理的な力を利用して分離を行います。これらの手法には、遠心分離、ろ過、篩分け(スクリーニング)プロセスが含まれ、化学反応や相変化を伴わず動作します。特にデカンタ遠心分離機などの遠心分離装置は、製薬製造において液体相から固体粒子を分離する際に優れた性能を発揮します。
機械式医薬品分離技術の選択は、粒子サイズ分布、相間の密度差、および要求される分離効率に依存します。これらのシステムは、連続運転、スケーラビリティ、および化学的汚染の最小化という点で優れた利点を提供し、化学的完全性の維持が極めて重要となる医薬中間体および最終製品の処理に適しています。
機械式分離法はまた、遠心力(G-force)、滞留時間、および処理能力などの運転パラメーターを優れた精度で制御できます。このような制御により、製薬メーカーは分離性能を最適化しつつ、一貫した製品品質を維持し、製薬用プロセス装置に関する規制要件を満たすことが可能になります。
化学的およびクロマトグラフィーによる分離法
医薬品分離技術における化学的分離手法には、目的化合物と不純物との間の化学的性質の差を活用した選択的溶解、沈殿、または抽出プロセスが含まれます。これらの手法は、機械的手法に比べて通常高い選択性を提供しますが、化学的適合性および下流工程における処理要件を慎重に検討する必要があります。
クロマトグラフィーによる医薬品分離技術は、医薬品の有効成分(API)の精製および構造的に類似した不純物の除去に対して極めて高い精度を実現します。これらのシステムでは、固定相および移動相を用いて分子間相互作用に基づく選択的分離を行いますが、通常はバッチ方式で運転され、最適化および保守には専門的な知識が求められます。
化学的手法とクロマトグラフィー手法の選択は、要求される純度レベル、操作規模、および経済的要因に依存します。これらの医薬品分離技術は非常に高い選択性を達成できますが、機械的分離手法と比較して、通常、運用コストが高くなり、プロセス制御もより複雑になります。
プロセス要件および仕様の評価
製品品質および純度基準
医薬品分離技術は、薬局方基準および規制当局によって定められた特定の純度要件に基づいて選択する必要があります。目標純度レベルは、分離システムの複雑さおよびコストに直接影響を与え、より高い純度要件は通常、複数段階の分離またはより高度な技術を必要とします。
原料に含まれる不純物の性質および濃度を理解することは、適切な医薬品分離技術を選択する上で不可欠です。一部の不純物は特定の分離メカニズムを必要とする一方で、他の不純物は高性能遠心分離機や高度なろ過システムなどの汎用分離装置を用いて効果的に除去できます。
分離性能の検証に用いる分析法も、医薬品分離技術を選定する際に考慮しなければなりません。選択された分離システムは、識別、純度および効力に関する既存の規格を満たすとともに、標準的な医薬品試験法を用いて容易に分析可能な製品を生成する必要があります。
生産規模および処理能力要件
生産量の要件は、製薬分離技術の選択に大きく影響します。これは、異なる技術がそれぞれ異なったスケーラビリティ特性および処理能力を有するためです。小規模な実験室レベルでの分離には、大規模な商業生産とは異なるアプローチが用いられる場合があり、スケールアップの実現可能性を慎重に検討する必要があります。
連続式操作とバッチ式操作のどちらを好むかという点も、製薬分離技術の選択に影響を与えます。連続式分離システム(例: 製薬分離技術 デカンタ遠心機を用いるもの)は、大量生産において優れた利点を提供しますが、一方でバッチ式システムは、特殊用途または高付加価値製品に対してより精密な制御を可能にします。
医薬品分離技術を選定する際には、変動する供給原料の組成および生産スケジュールに対応できる柔軟性を評価する必要があります。供給原料の特性や生産要件の変化に適応可能なシステムは、運用上の利点を提供し、製造全体の効率最適化を支援します。
規制およびコンプライアンスに関する考慮事項
優良製造規範の要求事項
すべての医薬品分離技術は、医薬品製造施設における設備設計、運転および保守を規定する「優良製造規範(GMP)」ガイドラインを遵守しなければなりません。これらの要件には、構造材料、表面仕上げ、洗浄手順および製品品質と患者安全を確保するための文書管理システムに関する仕様が含まれます。
医薬品分離技術のバリデーション要件には、機器が予め定められた仕様を満たす製品を一貫して生産することを証明するための包括的な試験および文書化が含まれます。このプロセスには、商業運転開始前に完了しなければならない、設置適格性確認(IQ)、運転適格性確認(OQ)、性能適格性確認(PQ)の各フェーズが含まれます。
医薬品分離技術においては、運転パラメーター、保守手順、または機器構成への変更を管理するための変更管理手順を確立する必要があります。これらの手順により、すべての変更が適切に評価・承認・記録され、規制対応性および製品品質が維持されることを保証します。
文書管理およびトレーサビリティ基準
医薬品分離技術では、機器の性能、保守作業、および製品ライフサイクル全体にわたる工程パラメーターを追跡する包括的な文書管理システムが必要です。これらの記録は、規制要件に従って維持され、規制当局による検査のために随時提示できる状態でなければなりません。
医薬品分離技術におけるトレーサビリティ要件には、各生産ロットについて原料、加工条件、および製品出力を詳細に記録することが含まれます。この情報により、品質問題の迅速な調査が可能となり、必要に応じて製品回収手順を支援します。
医薬品分離技術で使用される電子記録システムは、データ完全性に関する規制要件を遵守しなければならず、これには安全な保存、制御されたアクセス、および時間の経過に伴うすべてのデータ変更または削除を追跡する監査証跡(オーディットトレイル)の確保が含まれます。
経済的および運用上の要因
資本投資と運転コスト
医薬品分離技術の総所有コスト(TCO)には、初期の機器購入費用、設置費用、継続的な保守費用、および機器のライフサイクル全体にわたるユーティリティ(電力・水・圧縮空気など)消費費用が含まれます。これらのコストは、想定される生産量および製品のマージンと照らし合わせて評価し、経済的採算性を判断する必要があります。
医薬品分離技術の運用コストには、消耗品費、エネルギー消費費、人件費、および廃棄物処理費用が含まれます。省エネルギー型分離システムは、特に高スループット運転において、ユーティリティ費用が運用費用の大きな割合を占める場合に、機器の寿命期間を通じて大幅なコスト削減を実現できます。
医薬品分離技術の保守コストは、装置の複雑さ、運用環境、および保守要件に応じて大きく異なります。単純な機械式分離システムは、専門的な技術支援および交換用部品を必要とする複雑なクロマトグラフィー分離システムや化学的分離システムと比較して、通常、より低い保守コストを実現します。
技術のライフサイクルおよび陳腐化リスク
医薬品分離技術の予想耐用年数は、対象製品のライフサイクルおよび規制環境を踏まえて評価する必要があります。長寿命であり、確立されたサプライヤー支援を備えた技術は、長期的な価値が高く、重要な生産期間中に陳腐化するリスクが低減されます。
医薬品分離技術を選定する際には、サプライヤーの安定性および技術サポートの可用性が極めて重要な要素です。設備メーカーは、設備のライフサイクル全体にわたり、スペアパーツの供給、技術的支援、および規制対応に関する最新情報の提供を継続的に実施する必要があります。
医薬品分離技術を導入する際には、将来的な技術アップグレードの道筋を検討することが重要です。これにより、生産要件の変化や新たな規制要件の施行に応じて、設備を完全に交換することなく、改造または機能強化を行うことが可能になります。
導入および最適化戦略
既存の製造システムとの統合
医薬品分離技術を成功裏に導入するためには、既存の製造インフラ(上流および下流工程、ユーティリティシステム、制御システムを含む)との慎重な統合が必要です。この統合によって、素材のスムーズな流れとプロセス全体の最適な効率性が確保されるとともに、製品品質基準の維持が可能となります。
制御システムの互換性は、製薬分離技術を既存の製造設備に統合する際に不可欠です。最新の分離システムは、工場全体の制御および監視システムとのシームレスな統合を可能にする標準化された通信プロトコルおよびデータインターフェースを提供する必要があります。
製薬分離技術におけるオペレーターの訓練要件を評価し、安全かつ効果的な機器操作に必要な専門知識が確保されていることを確認する必要があります。訓練プログラムには、通常運転、トラブルシューティング、保守手順、および選定された分離技術に特有の緊急時対応手順が含まれる必要があります。
パフォーマンス監視および最適化
製薬分離技術向けの連続監視システムにより、分離性能のリアルタイム評価および製品品質に影響を及ぼす可能性のある問題の早期検出が可能になります。これらのシステムでは、分離効率、処理能力(スループット)、製品品質パラメーターなどの主要業績評価指標(KPI)を追跡する必要があります。
医薬品分離技術のプロセス最適化とは、分離性能を最大化するとともに運用コストを最小化し、かつ規制要件への準拠を維持するため、運転パラメーターを体系的に評価することを意味します。この最適化は、統計的に設計された実験および検証済みの分析法に基づいて実施されるべきです。
医薬品分離技術における定期的なパフォーマンスレビューは、改善機会の特定および変化する規制要件への継続的な準拠確保を支援します。これらのレビューには、プロセスデータ、保守記録、製品品質の傾向分析が含まれ、継続的改善活動を支える必要があります。
よくあるご質問(FAQ)
医薬品分離技術を選定する際に最も重要な要素は何ですか?
最も重要な要因には、規制遵守要件、製品純度仕様、生産規模、および総所有コスト(TCO)が含まれます。選定された技術は、優良製造規範(GMP)基準を満たすと同時に、所定の分離効率を達成し、対象となる生産量において経済的実行可能性を維持する必要があります。
規制要件は、医薬品分離技術の選定にどのように影響しますか?
規制要件により、医薬品分離技術は、機器の検証、文書管理システム、変更管理手順を含む優良製造規範(GMP)ガイドラインを遵守することが義務付けられます。これらの要件は、既に確立されており規制当局による承認実績があり、検証活動に対する包括的なベンダー支援が得られる技術を優先的に選択する傾向があります。
新しい医薬品分離技術を導入する際の通常の検証期間はどのくらいですか?
医薬品分離技術のバリデーション期間は、通常、装置の複雑さおよび規制要件に応じて6~18か月程度です。この期間には、導入適合性確認(IQ)、運転適合性確認(OQ)、性能適合性確認(PQ)、およびプロセスバリデーションの各フェーズが含まれ、商業生産開始前にすべて完了する必要があります。
医薬品分離技術の長期的な実用性をどのように評価しますか?
長期的な実用性の評価には、技術の成熟度、サプライヤーの安定性、保守・点検要件、および規制当局による承認状況が考慮されます。実績が豊富で、信頼性の高いサプライヤーサポートが得られ、今後の規制動向にも対応可能な技術は、医薬品製造業務においてより優れた長期的価値を提供し、陳腐化リスクを低減します。