Die Auswahl der richtigen pharmazeutischen Trenntechnologien ist eine entscheidende Entscheidung, die sich unmittelbar auf die Produktqualität, die Einhaltung behördlicher Vorschriften und die betriebliche Effizienz in der pharmazeutischen Produktion auswirkt. Bei der Auswahl müssen mehrere Faktoren bewertet werden, darunter die spezifischen zu verarbeitenden Verbindungen, die erforderlichen Reinheitsgrade, die Produktionsmengen sowie die behördlichen Anforderungen, die pharmazeutische Herstellungsprozesse regeln.

Die pharmazeutische Industrie ist auf präzise Trennverfahren angewiesen, um sicherzustellen, dass die Wirkstoffe strenge Qualitätsstandards erfüllen, ohne dabei Kosteneffizienz und Skalierbarkeit zu beeinträchtigen. Das Verständnis des Entscheidungsrahmens für pharmazeutische Trenntechnologien ermöglicht es Herstellern, ihre Prozesse zu optimieren, Kontaminationsrisiken zu reduzieren und konsistente Produktspezifikationen zu erreichen, die sowohl regulatorischen Zulassungsanforderungen als auch kommerziellen Erfordernissen genügen.
Verständnis der Kategorien pharmazeutischer Trenntechnologien
Mechanische Trennungsverfahren
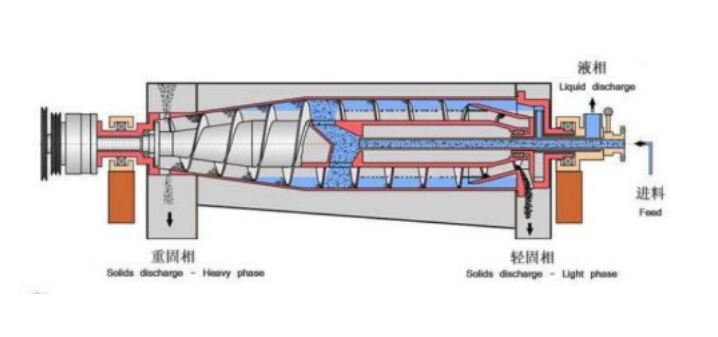
Mechanische pharmazeutische Trenntechnologien nutzen physikalische Kräfte, um Partikel anhand von Unterschieden in Größe, Dichte oder Form zu trennen. Zu diesen Verfahren zählen Zentrifugation, Filtration und Siebprozesse, die ohne chemische Reaktionen oder Phasenübergänge arbeiten. Zentrifugaltrenner – insbesondere Dekanterzentrifugen – zeichnen sich besonders durch ihre Leistungsfähigkeit bei der Trennung fester Partikel aus flüssigen Phasen in der pharmazeutischen Produktion aus.
Die Auswahl mechanischer pharmazeutischer Trenntechnologien hängt von der Partikelgrößenverteilung, den Dichteunterschieden zwischen den Phasen und dem erforderlichen Trenngrad ab. Diese Systeme bieten Vorteile hinsichtlich des kontinuierlichen Betriebs, der Skalierbarkeit und einer minimalen chemischen Kontamination und eignen sich daher für die Verarbeitung pharmazeutischer Zwischenprodukte und Endprodukte, bei denen die Aufrechterhaltung der chemischen Integrität von zentraler Bedeutung ist.
Mechanische Trennverfahren ermöglichen zudem eine ausgezeichnete Steuerung der Betriebsparameter wie Zentrifugalkraft (G-Kraft), Verweilzeit und Durchsatzraten. Diese Steuerung erlaubt pharmazeutischen Herstellern, die Trennleistung zu optimieren, gleichzeitig eine konsistente Produktqualität sicherzustellen und die regulatorischen Anforderungen an pharmazeutische Verarbeitungsanlagen zu erfüllen.
Chemische und chromatographische Trennverfahren
Chemische Trennverfahren in der pharmazeutischen Trenntechnik umfassen selektive Lösungs-, Fällungs- oder Extraktionsprozesse, die sich auf Unterschiede in den chemischen Eigenschaften zwischen Zielverbindungen und Verunreinigungen stützen. Diese Methoden bieten oft eine höhere Selektivität als mechanische Verfahren, erfordern jedoch sorgfältige Berücksichtigung der chemischen Verträglichkeit sowie der Anforderungen an die nachgeschaltete Aufbereitung.
Chromatographische pharmazeutische Trennverfahren bieten außergewöhnliche Präzision bei der Reinigung pharmazeutisch wirksamer Inhaltsstoffe und beim Entfernen eng verwandter Verunreinigungen. Diese Systeme nutzen stationäre und mobile Phasen, um eine selektive Trennung auf der Grundlage molekularer Wechselwirkungen zu erreichen; sie arbeiten jedoch typischerweise im Batch-Betrieb und erfordern spezialisiertes Fachwissen für Optimierung und Wartung.
Die Wahl zwischen chemischen und chromatographischen Verfahren hängt von den erforderlichen Reinheitsgraden, dem Betriebsumfang und wirtschaftlichen Überlegungen ab. Obwohl diese pharmazeutischen Trenntechnologien eine sehr hohe Selektivität erreichen können, sind sie oft mit höheren Betriebskosten und einer komplexeren Prozesssteuerung im Vergleich zu mechanischen Trennverfahren verbunden.
Bewertung der Prozessanforderungen und -spezifikationen
Produktqualität und Reinheitsstandards
Pharmazeutische Trenntechnologien müssen anhand der spezifischen Reinheitsanforderungen ausgewählt werden, die durch Pharmakopöen und zuständige Aufsichtsbehörden festgelegt sind. Der angestrebte Reinheitsgrad beeinflusst unmittelbar die Komplexität und die Kosten des Trennsystems; höhere Reinheitsanforderungen erfordern in der Regel mehrere Trennstufen oder anspruchsvollere Technologien.
Das Verständnis der Art und Konzentration der Verunreinigungen im Ausgangsmaterial ist entscheidend für die Auswahl geeigneter pharmazeutischer Trenntechnologien. Einige Verunreinigungen erfordern spezifische Trennmechanismen, während andere effektiv mit universell einsetzbaren Trennvorrichtungen wie Hochleistungs-Zentrifugen oder fortschrittlichen Filtrationssystemen entfernt werden können.
Auch die analytischen Methoden, die zur Überprüfung der Trennleistung eingesetzt werden, müssen bei der Auswahl pharmazeutischer Trenntechnologien berücksichtigt werden. Das gewählte Trennsystem muss Produkte liefern, die sich mithilfe gängiger pharmazeutischer Prüfmethoden problemlos analysieren lassen und gleichzeitig die festgelegten Spezifikationen hinsichtlich Identität, Reinheit und Wirksamkeit erfüllen.
Produktionsumfang und Durchsatzanforderungen
Die Anforderungen an das Produktionsvolumen beeinflussen die Auswahl pharmazeutischer Trenntechnologien erheblich, da verschiedene Technologien unterschiedliche Skalierbarkeitseigenschaften und Durchsatzkapazitäten aufweisen. Kleinskalige Labor-Trennungen können andere Ansätze nutzen als großtechnische kommerzielle Produktion, was eine sorgfältige Abwägung der Hochskalierbarkeit erfordert.
Die Präferenz für kontinuierliche oder diskontinuierliche (Batch-)Betriebsweise wirkt sich ebenfalls auf die Wahl pharmazeutischer Trenntechnologien aus. Kontinuierliche Trennsysteme wie pharmazeutische Trenntechnologien mit Dekanter-Zentrifugen bieten Vorteile für die Hochvolumenproduktion, während Batch-Systeme bei Spezial- oder hochwertigen Produkten eine bessere Prozesskontrolle ermöglichen.
Die Flexibilität, unterschiedliche Zusammensetzungen der Zulaufstoffe und Produktionspläne zu bewältigen, sollte bei der Auswahl pharmazeutischer Trenntechnologien bewertet werden. Systeme, die Änderungen in den Eigenschaften des Zulaufs oder in den Produktionsanforderungen berücksichtigen können, bieten betriebliche Vorteile und tragen zur Optimierung der gesamten Fertigungseffizienz bei.
Regulatorische und Compliance-Aspekte
Anforderungen der Guten Herstellungspraxis
Alle pharmazeutischen Trenntechnologien müssen den Richtlinien der Good Manufacturing Practice (GMP) entsprechen, die das Design, den Betrieb und die Wartung von Anlagen in pharmazeutischen Produktionsstätten regeln. Zu diesen Anforderungen gehören Spezifikationen für Konstruktionsmaterialien, Oberflächenbeschaffenheit, Reinigungsverfahren sowie Dokumentationssysteme, die Qualität des Produkts und die Sicherheit der Patienten gewährleisten.
Die Validierungsanforderungen für pharmazeutische Trenntechnologien umfassen umfassende Prüfungen und Dokumentationen, um nachzuweisen, dass die Anlagen konsistent Produkte herstellen, die vorab festgelegten Spezifikationen entsprechen. Dieser Prozess umfasst die Phasen der Installation Qualification (IQ), Operational Qualification (OQ) und Performance Qualification (PQ), die vor dem kommerziellen Betrieb abgeschlossen sein müssen.
Für pharmazeutische Trenntechnologien müssen Änderungskontrollverfahren etabliert werden, um Modifikationen an Betriebsparametern, Wartungsverfahren oder Gerätekonfigurationen zu steuern. Diese Verfahren stellen sicher, dass alle Änderungen ordnungsgemäß bewertet, genehmigt und dokumentiert werden, um die Einhaltung behördlicher Vorgaben und die Produktqualität zu gewährleisten.
Dokumentations- und Rückverfolgbarkeitsstandards
Pharmazeutische Trenntechnologien erfordern umfassende Dokumentationssysteme, die die Geräteleistung, Wartungsaktivitäten und Prozessparameter während des gesamten Produktlebenszyklus verfolgen. Diese Aufzeichnungen müssen gemäß den regulatorischen Anforderungen geführt und für Inspektionen durch die zuständigen Behörden zugänglich gehalten werden.
Die Rückverfolgbarkeitsanforderungen für pharmazeutische Trenntechnologien umfassen die Führung detaillierter Aufzeichnungen über Einsatzstoffe, Verarbeitungsbedingungen und Produktausgänge für jede Produktionscharge. Diese Informationen ermöglichen eine schnelle Untersuchung von Qualitätsproblemen und unterstützen gegebenenfalls Maßnahmen zur Rückrufung von Produkten.
Elektronische Aufzeichnungssysteme, die mit pharmazeutischen Trenntechnologien eingesetzt werden, müssen den regulatorischen Anforderungen an die Datenechtheit entsprechen, einschließlich Regelungen für sichere Speicherung, kontrollierten Zugriff sowie Audit-Trails, die sämtliche Datenänderungen oder -löschungen im Zeitverlauf nachvollziehbar dokumentieren.
Wirtschaftliche und betriebliche Faktoren
Kapitalinvestitionen und Betriebskosten
Die Gesamtbetriebskosten für pharmazeutische Trenntechnologien umfassen den Anschaffungspreis der Anlagen, Installationskosten, laufende Wartungskosten sowie den Energieverbrauch während der gesamten Lebensdauer der Ausrüstung. Diese Kosten müssen im Verhältnis zu den erwarteten Produktionsmengen und Produktmargen bewertet werden, um die wirtschaftliche Tragfähigkeit zu bestimmen.
Zu den Betriebskosten für pharmazeutische Trenntechnologien zählen Verbrauchsmaterialien, Energieverbrauch, Personalaufwand sowie Kosten für die Entsorgung von Abfällen. Energiesparende Trennsysteme können über die gesamte Lebensdauer der Anlagen erhebliche Kosteneinsparungen ermöglichen, insbesondere bei Hochleistungsanwendungen, bei denen die Energiekosten einen erheblichen Anteil der Betriebskosten ausmachen.
Die Wartungskosten für pharmazeutische Trenntechnologien variieren erheblich je nach Gerätekomplexität, Betriebsumgebung und Wartungsanforderungen. Einfache mechanische Trennsysteme weisen in der Regel niedrigere Wartungskosten auf als komplexe chromatographische oder chemische Trennsysteme, die spezialisierte technische Unterstützung und Ersatzkomponenten erfordern.
Technologie-Lebenszyklus und Obsoleszenzrisiko
Die erwartete Nutzungsdauer pharmazeutischer Trenntechnologien sollte im Hinblick auf den prognostizierten Produktlebenszyklus sowie das regulatorische Umfeld bewertet werden. Technologien mit langer Nutzungsdauer und etablierter Lieferantensupport bieten einen höheren langfristigen Wert und verringern das Risiko einer Obsoleszenz während kritischer Produktionsphasen.
Die Stabilität des Lieferanten und die Verfügbarkeit technischer Unterstützung sind entscheidende Faktoren bei der Auswahl pharmazeutischer Trenntechnologien, da Gerätehersteller während des gesamten Lebenszyklus der Ausrüstung eine kontinuierliche Unterstützung hinsichtlich Ersatzteilen, technischer Hilfe und Aktualisierungen zur Einhaltung behördlicher Vorschriften bereitstellen müssen.
Bei der Implementierung pharmazeutischer Trenntechnologien sollten Technologie-Upgrade-Pfade berücksichtigt werden, um sicherzustellen, dass die Ausrüstung angepasst oder erweitert werden kann, sobald sich die Produktionsanforderungen ändern oder neue behördliche Anforderungen eingeführt werden – ohne dass ein vollständiger Austausch erforderlich ist.
Implementierungs- und Optimierungsstrategien
Integration in bestehende Fertigungssysteme
Eine erfolgreiche Implementierung pharmazeutischer Trenntechnologien erfordert eine sorgfältige Integration in die bestehende Fertigungsinfrastruktur, einschließlich vorgelagerter und nachgelagerter Prozesse, Versorgungssysteme und Leitsysteme. Diese Integration gewährleistet einen reibungslosen Materialfluss und eine optimale Gesamtprozesseffizienz bei gleichzeitiger Einhaltung der Qualitätsstandards für das Produkt.
Die Kompatibilität des Steuerungssystems ist entscheidend, wenn pharmazeutische Trenntechnologien in bestehende Produktionsanlagen integriert werden. Moderne Trennsysteme sollten standardisierte Kommunikationsprotokolle und Daten-Schnittstellen bereitstellen, die eine nahtlose Integration in unternehmensweite Steuerungs- und Überwachungssysteme ermöglichen.
Die Anforderungen an die Bedienerausbildung für pharmazeutische Trenntechnologien müssen bewertet werden, um sicherzustellen, dass ausreichende Fachkenntnisse für einen sicheren und effektiven Betrieb der Anlagen vorliegen. Die Schulungsprogramme sollten den Regelbetrieb, die Fehlerbehebung, Wartungsverfahren sowie Notfallreaktionsprotokolle abdecken, die spezifisch für die ausgewählte Trenntechnologie sind.
Leistungsüberwachung und Optimierung
Kontinuierliche Überwachungssysteme für pharmazeutische Trenntechnologien ermöglichen die Echtzeiteinschätzung der Trennleistung und die frühzeitige Erkennung potenzieller Probleme, die die Produktqualität beeinträchtigen könnten. Diese Systeme sollten wesentliche Leistungsindikatoren wie Trenneffizienz, Durchsatzraten und Produktqualitätsparameter erfassen.
Die Prozessoptimierung für pharmazeutische Trenntechnologien umfasst die systematische Bewertung von Betriebsparametern, um die Trennleistung zu maximieren, die Betriebskosten zu minimieren und die Einhaltung gesetzlicher Vorschriften sicherzustellen. Diese Optimierung sollte auf statistisch geplanten Experimenten und validierten analytischen Methoden beruhen.
Regelmäßige Leistungsüberprüfungen für pharmazeutische Trenntechnologien helfen dabei, Verbesserungspotenziale zu identifizieren und die fortlaufende Einhaltung sich weiterentwickelnder regulatorischer Anforderungen sicherzustellen. Zu diesen Überprüfungen gehören die Analyse von Prozessdaten, Wartungsunterlagen und Trends zur Produktqualität, um Initiativen zur kontinuierlichen Verbesserung zu unterstützen.
Häufig gestellte Fragen
Welche Faktoren sind bei der Auswahl pharmazeutischer Trenntechnologien am kritischsten?
Zu den entscheidendsten Faktoren zählen die Anforderungen an die regulatorische Konformität, Spezifikationen zur Produktreinheit, der Produktionsumfang sowie die Gesamtbetriebskosten. Die ausgewählte Technologie muss die Good-Manufacturing-Practice-(GMP-)Standards erfüllen und gleichzeitig die erforderliche Trenneffizienz erreichen sowie für die vorgesehenen Produktionsmengen wirtschaftlich tragfähig bleiben.
Wie beeinflussen regulatorische Anforderungen die Auswahl pharmazeutischer Trenntechnologien?
Regulatorische Anforderungen schreiben vor, dass pharmazeutische Trenntechnologien den Good-Manufacturing-Practice-(GMP-)Richtlinien entsprechen müssen, darunter die Validierung von Anlagen, Dokumentationssysteme und Verfahren zur Änderungskontrolle. Diese Anforderungen begünstigen häufig etablierte Technologien mit nachgewiesener regulatorischer Akzeptanz sowie umfassender Unterstützung durch den Lieferanten bei Validierungsaktivitäten.
Wie lange dauert in der Regel die Validierung bei der Einführung neuer pharmazeutischer Trenntechnologien?
Die Validierungszeiträume für pharmazeutische Trenntechnologien liegen typischerweise zwischen 6 und 18 Monaten, abhängig von der Komplexität der Anlagen und den regulatorischen Anforderungen. Dieser Zeitraum umfasst die Installation Qualification (IQ), Operational Qualification (OQ), Performance Qualification (PQ) sowie die Prozessvalidierung, die alle vor Beginn der kommerziellen Produktion abgeschlossen sein müssen.
Wie bewerten Sie die langfristige Lebensfähigkeit pharmazeutischer Trenntechnologien?
Bei der Bewertung der langfristigen Lebensfähigkeit werden die Reife der Technologie, die Stabilität des Lieferanten, die Wartungsanforderungen sowie die regulatorische Akzeptanz berücksichtigt. Technologien mit nachgewiesener Einsatzhistorie, zuverlässiger Lieferantensupport und Kompatibilität mit aktuellen regulatorischen Trends bieten einen höheren langfristigen Nutzen und reduzieren das Risiko einer Obsoleszenz für pharmazeutische Fertigungsprozesse.
Inhaltsverzeichnis
- Verständnis der Kategorien pharmazeutischer Trenntechnologien
- Bewertung der Prozessanforderungen und -spezifikationen
- Regulatorische und Compliance-Aspekte
- Wirtschaftliche und betriebliche Faktoren
- Implementierungs- und Optimierungsstrategien
-
Häufig gestellte Fragen
- Welche Faktoren sind bei der Auswahl pharmazeutischer Trenntechnologien am kritischsten?
- Wie beeinflussen regulatorische Anforderungen die Auswahl pharmazeutischer Trenntechnologien?
- Wie lange dauert in der Regel die Validierung bei der Einführung neuer pharmazeutischer Trenntechnologien?
- Wie bewerten Sie die langfristige Lebensfähigkeit pharmazeutischer Trenntechnologien?