Le choix des bonnes technologies de séparation pharmaceutique est une décision critique qui a un impact direct sur la qualité du produit, le respect des réglementations et l’efficacité opérationnelle dans la fabrication pharmaceutique. Ce choix implique l’évaluation de plusieurs facteurs, notamment les composés spécifiques traités, les niveaux de pureté requis, les volumes de production et les exigences réglementaires encadrant les procédés de fabrication pharmaceutique.

L'industrie pharmaceutique repose sur des méthodes de séparation précises afin de garantir que les principes actifs répondent à des normes de qualité rigoureuses, tout en préservant l'efficacité économique et la possibilité d'élargissement à grande échelle. La compréhension du cadre décisionnel relatif aux technologies de séparation pharmaceutique permet aux fabricants d'optimiser leurs procédés, de réduire les risques de contamination et d'atteindre des spécifications produit constantes, conformes tant aux exigences réglementaires qu'aux impératifs de viabilité commerciale.
Comprendre les catégories de technologies de séparation pharmaceutique
Technologies de Séparation Mécanique
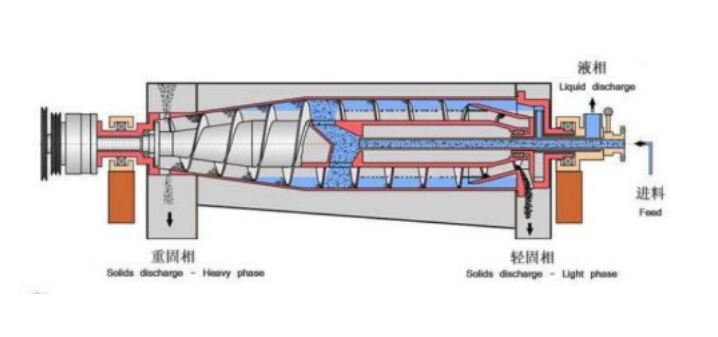
Les technologies mécaniques de séparation pharmaceutique utilisent des forces physiques pour séparer les particules en fonction de différences de taille, de densité ou de forme. Ces méthodes comprennent la centrifugation, la filtration et les procédés de tamisage, qui s'effectuent sans réaction chimique ni changement de phase. Les séparateurs centrifuges, notamment les centrifugeuses décanteuses, se distinguent particulièrement dans la séparation des particules solides des phases liquides en fabrication pharmaceutique.
Le choix des technologies mécaniques de séparation pharmaceutique dépend de la distribution granulométrique, des différences de densité entre les phases et de l’efficacité de séparation requise. Ces systèmes présentent des avantages en termes de fonctionnement continu, d’évolutivité et de contamination chimique minimale, ce qui les rend adaptés au traitement des intermédiaires pharmaceutiques et des produits finaux, où le maintien de l’intégrité chimique est primordial.
Les méthodes de séparation mécanique permettent également un excellent contrôle des paramètres opératoires tels que la force centrifuge (G-force), le temps de séjour et les débits. Ce contrôle permet aux fabricants pharmaceutiques d’optimiser les performances de séparation tout en assurant une qualité constante du produit et en respectant les exigences réglementaires applicables aux équipements de traitement pharmaceutique.
Méthodes chimiques et chromatographiques de séparation
Les approches de séparation chimique dans les technologies de séparation pharmaceutique impliquent des procédés de dissolution sélective, de précipitation ou d’extraction qui exploitent les différences de propriétés chimiques entre les composés cibles et les impuretés. Ces méthodes offrent souvent une sélectivité supérieure à celle des approches mécaniques, mais nécessitent une attention particulière portée à la compatibilité chimique ainsi qu’aux exigences de traitement en aval.
Les technologies de séparation pharmaceutique par chromatographie offrent une précision exceptionnelle pour la purification des principes actifs pharmaceutiques et l’élimination d’impuretés étroitement apparentées. Ces systèmes utilisent des phases stationnaires et mobiles afin d’obtenir une séparation sélective fondée sur les interactions moléculaires, bien qu’ils fonctionnent généralement en mode discontinu et requièrent une expertise spécialisée pour leur optimisation et leur maintenance.
Le choix entre les méthodes chimiques et chromatographiques dépend des niveaux de pureté requis, de l’échelle d’exploitation et des considérations économiques. Bien que ces technologies de séparation pharmaceutique puissent atteindre une sélectivité très élevée, elles impliquent souvent des coûts d’exploitation plus élevés et un contrôle de procédé plus complexe par rapport aux approches de séparation mécanique.
Évaluation des exigences et des spécifications du procédé
Normes de qualité et de pureté du produit
Les technologies de séparation pharmaceutique doivent être sélectionnées en fonction des exigences spécifiques de pureté établies par les normes pharmacopéiques et les autorités réglementaires. Le niveau de pureté cible influence directement la complexité et le coût du système de séparation, des exigences de pureté plus élevées nécessitant généralement plusieurs étapes de séparation ou des technologies plus sophistiquées.
Comprendre la nature et la concentration des impuretés présentes dans la matière première est essentiel pour choisir les technologies pharmaceutiques de séparation adaptées. Certaines impuretés peuvent nécessiter des mécanismes de séparation spécifiques, tandis que d'autres peuvent être efficacement éliminées à l'aide d'équipements de séparation polyvalents, tels que des centrifugeuses haute performance ou des systèmes de filtration avancés.
Les méthodes analytiques utilisées pour vérifier les performances de séparation doivent également être prises en compte lors de la sélection des technologies pharmaceutiques de séparation. Le système de séparation retenu doit produire des produits pouvant être facilement analysés à l’aide des méthodes d’essai pharmaceutiques standard, tout en respectant les spécifications établies en matière d’identité, de pureté et de puissance.
Échelle de production et exigences de débit
Les exigences en matière de volume de production influencent considérablement le choix des technologies de séparation pharmaceutique, car les différentes technologies présentent des caractéristiques de montée en échelle et des capacités de débit variables. Les séparations à petite échelle en laboratoire peuvent faire appel à des approches différentes de celles utilisées dans la production commerciale à grande échelle, ce qui nécessite une réflexion attentive sur la faisabilité du passage à l’échelle.
Les préférences entre fonctionnement continu et fonctionnement par lots influencent également le choix des technologies de séparation pharmaceutique. Les systèmes de séparation continue, tels que technologies de séparation pharmaceutique l’utilisation de centrifugeuses décanteuses, offrent des avantages pour la production à haut volume, tandis que les systèmes par lots peuvent assurer un meilleur contrôle pour les produits spécialisés ou à forte valeur ajoutée.
La flexibilité permettant de traiter des compositions d’alimentation variables et des plannings de production doit être évaluée lors du choix des technologies de séparation pharmaceutique. Les systèmes capables de s’adapter aux changements des caractéristiques de l’alimentation ou aux exigences de production offrent des avantages opérationnels et contribuent à optimiser l’efficacité globale de la fabrication.
Considérations réglementaires et de conformité
Exigences de bonnes pratiques de fabrication
Toutes les technologies de séparation pharmaceutique doivent respecter les bonnes pratiques de fabrication (BPF), qui régissent la conception, l’exploitation et la maintenance des équipements dans les installations de fabrication pharmaceutique. Ces exigences comprennent des spécifications relatives aux matériaux de construction, aux finitions de surface, aux procédures de nettoyage et aux systèmes de documentation garantissant la qualité du produit et la sécurité des patients.
Les exigences de validation des technologies de séparation pharmaceutique impliquent des essais et une documentation complets afin de démontrer que l’équipement produit systématiquement des produits conformes aux spécifications prédéterminées. Ce processus comprend les phases de qualification d’installation, de qualification opérationnelle et de qualification de performance, qui doivent être menées à bien avant la mise en service commerciale.
Des procédures de maîtrise des changements doivent être établies pour les technologies de séparation pharmaceutique afin de gérer les modifications apportées aux paramètres de fonctionnement, aux procédures de maintenance ou aux configurations de l’équipement. Ces procédures garantissent qu’aucun changement n’est mis en œuvre sans avoir été correctement évalué, approuvé et documenté, afin de préserver la conformité réglementaire et la qualité du produit.
Normes de documentation et de traçabilité
Les technologies de séparation pharmaceutique exigent des systèmes de documentation complets permettant de suivre les performances des équipements, les activités de maintenance et les paramètres du procédé tout au long du cycle de vie du produit. Ces enregistrements doivent être tenus conformément aux exigences réglementaires et mis à la disposition des autorités réglementaires pour inspection.
Les exigences en matière de traçabilité applicables aux technologies de séparation pharmaceutique comprennent la tenue d’enregistrements détaillés relatifs aux matières premières entrantes, aux conditions de traitement et aux produits obtenus pour chaque lot de production. Ces informations permettent une investigation rapide des problèmes de qualité et soutiennent les procédures de rappel de produits, le cas échéant.
Les systèmes d’enregistrement électroniques utilisés avec les technologies de séparation pharmaceutique doivent respecter les exigences réglementaires relatives à l’intégrité des données, y compris des dispositions garantissant un stockage sécurisé, un accès contrôlé et des pistes d’audit permettant de suivre toutes les modifications ou suppressions de données dans le temps.
Facteurs économiques et opérationnels
Investissement en capital et coûts d'exploitation
Le coût total de possession des technologies de séparation pharmaceutique comprend l'achat initial des équipements, les coûts d'installation, les frais d'entretien courants et la consommation d'énergie tout au long du cycle de vie de l'équipement. Ces coûts doivent être évalués par rapport aux volumes de production attendus et aux marges bénéficiaires des produits afin de déterminer la viabilité économique.
Les coûts d'exploitation des technologies de séparation pharmaceutique englobent les consommables, la consommation d'énergie, les besoins en main-d'œuvre et les frais d'élimination des déchets. Les systèmes de séparation économes en énergie peuvent générer des économies substantielles sur la durée de vie de l'équipement, notamment dans le cas d'opérations à haut débit, où les coûts liés aux services publics représentent une part importante des dépenses d'exploitation.
Les coûts d'entretien des technologies de séparation pharmaceutique varient considérablement en fonction de la complexité des équipements, de l'environnement opérationnel et des exigences en matière d'entretien. Les systèmes de séparation mécanique simples offrent généralement des coûts d'entretien inférieurs à ceux des systèmes de séparation chromatographique ou chimique complexes, qui nécessitent un soutien technique spécialisé ainsi que des composants de remplacement.
Cycle de vie technologique et risque d'obsolescence
La durée de vie prévue des technologies de séparation pharmaceutique doit être évaluée par rapport au cycle de vie attendu du produit et à l'environnement réglementaire. Les technologies dotées d'une longue durée de vie et bénéficiant d'un soutien éprouvé de la part des fournisseurs offrent une plus grande valeur à long terme et réduisent le risque d'obsolescence pendant les périodes critiques de production.
La stabilité des fournisseurs et la disponibilité d’un soutien technique sont des facteurs cruciaux lors de la sélection des technologies de séparation pharmaceutique, car les fabricants d’équipements doivent assurer un soutien continu en matière de pièces détachées, d’assistance technique et de mises à jour liées à la conformité réglementaire tout au long du cycle de vie de l’équipement.
Les voies d’amélioration technologique doivent être prises en compte lors de la mise en œuvre des technologies de séparation pharmaceutique afin de garantir que les équipements puissent être modifiés ou améliorés à mesure que les exigences de production évoluent ou que de nouvelles exigences réglementaires sont mises en œuvre, sans qu’il soit nécessaire de les remplacer entièrement.
Stratégies de mise en œuvre et d'optimisation
Intégration avec les systèmes de fabrication existants
La mise en œuvre réussie des technologies de séparation pharmaceutique exige une intégration rigoureuse avec les infrastructures manufacturières existantes, y compris les procédés en amont et en aval, les systèmes utilitaires et les systèmes de commande. Cette intégration garantit un écoulement fluide des matières premières et une efficacité globale optimale du procédé, tout en préservant les normes de qualité du produit.
La compatibilité du système de contrôle est essentielle lors de l’intégration des technologies de séparation pharmaceutique avec les équipements de fabrication existants. Les systèmes modernes de séparation doivent offrir des protocoles de communication normalisés et des interfaces de données permettant une intégration transparente avec les systèmes de contrôle et de surveillance à l’échelle de l’usine.
Les besoins en formation des opérateurs pour les technologies de séparation pharmaceutique doivent être évalués afin de garantir la disponibilité d’une expertise adéquate pour une exploitation sûre et efficace des équipements. Les programmes de formation doivent couvrir le fonctionnement normal, la recherche et la résolution des pannes, les procédures de maintenance ainsi que les protocoles de réponse aux urgences spécifiques à la technologie de séparation retenue.
Surveillance et optimisation des performances
Les systèmes de surveillance continue pour les technologies de séparation pharmaceutique permettent une évaluation en temps réel des performances de séparation et une détection précoce des problèmes potentiels pouvant affecter la qualité du produit. Ces systèmes doivent suivre des indicateurs clés de performance tels que l’efficacité de séparation, les débits de production et les paramètres de qualité du produit.
L'optimisation des procédés pour les technologies de séparation pharmaceutique implique une évaluation systématique des paramètres opératoires afin de maximiser les performances de séparation tout en minimisant les coûts d'exploitation et en assurant le respect des exigences réglementaires.
Les revues régulières des performances des technologies de séparation pharmaceutique permettent d'identifier les possibilités d'amélioration et de garantir le maintien de la conformité aux exigences réglementaires en constante évolution. Ces revues doivent inclure l'analyse des données de procédé, des registres de maintenance et des tendances relatives à la qualité des produits afin de soutenir les initiatives d'amélioration continue.
FAQ
Quels sont les facteurs les plus critiques lors du choix des technologies de séparation pharmaceutique ?
Les facteurs les plus critiques comprennent les exigences en matière de conformité réglementaire, les spécifications de pureté des produits, l’échelle de production et le coût total de possession. La technologie retenue doit respecter les bonnes pratiques de fabrication tout en atteignant l’efficacité de séparation requise et en restant économiquement viable pour les volumes de production prévus.
Comment les exigences réglementaires influencent-elles la sélection des technologies de séparation pharmaceutique ?
Les exigences réglementaires imposent que les technologies de séparation pharmaceutique soient conformes aux lignes directrices relatives aux bonnes pratiques de fabrication, notamment en ce qui concerne la validation des équipements, les systèmes de documentation et les procédures de maîtrise des changements. Ces exigences privilégient souvent des technologies éprouvées, largement acceptées sur le plan réglementaire, et bénéficiant d’un soutien complet des fournisseurs en matière de validation.
Quel est le délai typique de validation pour la mise en œuvre de nouvelles technologies de séparation pharmaceutique ?
Les délais de validation des technologies de séparation pharmaceutique varient généralement de 6 à 18 mois, selon la complexité des équipements et les exigences réglementaires. Ce délai comprend les phases de qualification d’installation, de qualification opérationnelle, de qualification de performance et de validation du procédé, qui doivent toutes être achevées avant la production commerciale.
Comment évaluez-vous la viabilité à long terme des technologies de séparation pharmaceutique ?
L’évaluation de la viabilité à long terme prend en compte la maturité technologique, la stabilité des fournisseurs, les besoins en maintenance et l’acceptation réglementaire. Les technologies disposant d’un historique éprouvé, d’un soutien fiable de la part des fournisseurs et d’une compatibilité avec les tendances réglementaires émergentes offrent une meilleure valeur à long terme et réduisent le risque d’obsolescence pour les opérations de fabrication pharmaceutique.
Table des matières
- Comprendre les catégories de technologies de séparation pharmaceutique
- Évaluation des exigences et des spécifications du procédé
- Considérations réglementaires et de conformité
- Facteurs économiques et opérationnels
- Stratégies de mise en œuvre et d'optimisation
-
FAQ
- Quels sont les facteurs les plus critiques lors du choix des technologies de séparation pharmaceutique ?
- Comment les exigences réglementaires influencent-elles la sélection des technologies de séparation pharmaceutique ?
- Quel est le délai typique de validation pour la mise en œuvre de nouvelles technologies de séparation pharmaceutique ?
- Comment évaluez-vous la viabilité à long terme des technologies de séparation pharmaceutique ?