Valg af de rigtige farmaceutiske separationsteknologier er en afgørende beslutning, der direkte påvirker produktkvaliteten, overholdelse af reguleringskrav og den operative effektivitet i farmaceutisk fremstilling. Valget indebærer en vurdering af flere faktorer, herunder de specifikke forbindelser, der behandles, de krævede renhedsniveauer, produktionsmængderne og de reguleringskrav, der gælder for farmaceutiske fremstillingsprocesser.

Lægeindustrien er afhængig af præcise adskillelsesmetoder for at sikre, at aktive farmaceutiske ingredienser opfylder strenge kvalitetskrav, samtidig med at der opnås omkostningseffektivitet og skalerbarhed. At forstå beslutningsrammen for farmaceutiske adskillelsteknologier gør det muligt for producenter at optimere deres processer, reducere risikoen for forurening og opnå konsekvente produktspecifikationer, der opfylder både kravene til regulering og kommerciel levedygtighed.
Forståelse af kategorier inden for farmaceutisk adskillelsteknologi
Mekaniske Separationsteknologier
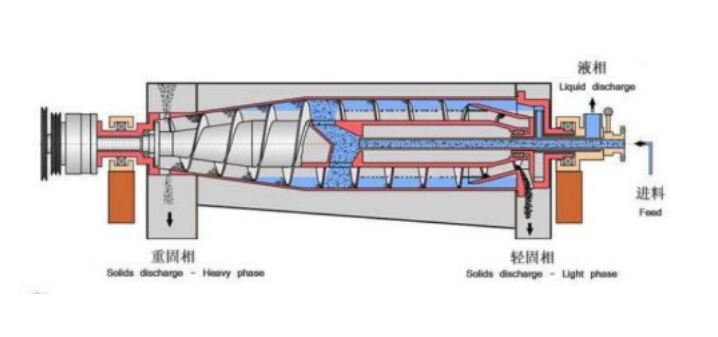
Mekaniske farmaceutiske adskillelsteknologier anvender fysiske kræfter til at adskille partikler på grundlag af forskelle i størrelse, densitet eller form. Disse metoder omfatter centrifugering, filtrering og sigteprocesser, der foregår uden kemiske reaktioner eller faseændringer. Centrifugalseparatorer, især dekantercentrifuger, udmærker sig ved at adskille faste partikler fra væskefaser i farmaceutisk fremstilling.
Valget af mekaniske farmaceutiske separationsmetoder afhænger af partikelstørrelsesfordelingen, densitetsforskellene mellem faserne og den krævede separationsydelse. Disse systemer har fordele i forbindelse med kontinuerlig drift, skalérbarhed og minimal kemisk forurening, hvilket gør dem velegnede til behandling af farmaceutiske mellemprodukter og færdige produkter, hvor det er afgørende at opretholde den kemiske integritet.
Mekaniske separationsmetoder giver også fremragende kontrol over driftsparametre såsom G-kraft, opholdstid og igennemstrømningshastigheder. Denne kontrol gør det muligt for farmaceutiske producenter at optimere separationsydelsen samtidig med, at de sikrer konsekvent produktkvalitet og opfylder regulatoriske krav til farmaceutisk procesudstyr.
Kemiske og kromatografiske separationsmetoder
Kemiske separationsmetoder inden for farmaceutiske separationsteknologier omfatter selektiv opløsning, fældning eller ekstraktion, der udnytter forskelle i kemiske egenskaber mellem målforbindelser og urenheder. Disse metoder giver ofte højere selektivitet end mekaniske metoder, men kræver omhyggelig overvejelse af kemisk kompatibilitet og krav til efterfølgende processtrin.
Kromatografiske farmaceutiske separationsteknologier tilbyder ekstraordinær præcision til rensning af aktive farmaceutiske ingredienser og fjernelse af tæt beslægtede urenheder. Disse systemer anvender stationære og mobile faser til at opnå selektiv separation baseret på molekylære interaktioner, selvom de typisk opererer i batchtilstand og kræver specialiseret ekspertise til optimering og vedligeholdelse.
Valget mellem kemiske og kromatografiske metoder afhænger af de krævede renhedsniveauer, driftsstørrelsen og økonomiske overvejelser. Selvom disse farmaceutiske separationsteknologier kan opnå meget høj selektivitet, indebærer de ofte højere driftsomkostninger og mere kompleks proceskontrol sammenlignet med mekaniske separationstilgange.
Vurdering af proceskrav og specifikationer
Produkkvalitet og renhedskrav
Farmaceutiske separationsteknologier skal vælges ud fra de specifikke renhedskrav, der er fastsat i farmakopéstandarder og af regulering myndigheder. Det målrettede renhedsniveau påvirker direkte kompleksiteten og omkostningerne ved separationssystemet, idet højere renhedskrav typisk kræver flere separationstrin eller mere avancerede teknologier.
At forstå arten og koncentrationen af urenheder i råmaterialet er afgørende for at vælge passende farmaceutiske separationsteknologier. Nogle urenheder kræver måske specifikke separationsmekanismer, mens andre kan fjernes effektivt ved hjælp af almindeligt anvendte separationssystemer, såsom højtydende centrifuger eller avancerede filtreringssystemer.
De analytiske metoder, der anvendes til at verificere separationens ydeevne, skal også overvejes ved valg af farmaceutiske separationsteknologier. Det valgte separationssystem skal frembringe produkter, der let kan analyseres ved hjælp af standardfarmaceutiske testmetoder, samtidig med at de opfylder de fastlagte specifikationer for identitet, renhed og styrke.
Produktionsstørrelse og gennemløbskrav
Produktionsvolumenkrav påvirker væsentligt valget af farmaceutiske separationsteknologier, da forskellige teknologier har forskellige skalbarhedsegenskaber og kapacitetsmuligheder. Laboratoriebaserede separationer i lille skala kan anvende andre metoder end kommerciel produktion i stor skala, hvilket kræver en omhyggelig vurdering af muligheden for at skala op.
Præferencer for kontinuerlig versus batch-drift påvirker også valget af farmaceutiske separationsteknologier. Kontinuerlige separationssystemer, såsom farmaceutiske separations teknologier der anvender dekantercentrifuger, tilbyder fordele ved produktion i høj mængde, mens batch-systemer kan give bedre kontrol ved special- eller højt-værdiprodukter.
Fleksibiliteten til at håndtere varierende fødematerialssammensætninger og produktionsplaner bør vurderes ved udvælgelsen af farmaceutiske separationsteknologier. Systemer, der kan tilpasse sig ændringer i fødematerialskarakteristika eller produktionskrav, giver operationelle fordele og hjælper med at optimere den samlede fremstillingseffektivitet.
Regulering og overholdelsesovervejelser
God Produktionsspraksis Krav
Alle farmaceutiske separationsteknologier skal overholde retningslinjerne for god fremstillingspraksis (GMP), som regulerer udstyrets design, drift og vedligeholdelse i farmaceutiske produktionsfaciliteter. Disse krav omfatter specifikationer for konstruktionsmaterialer, overfladeafslutninger, rengøringsprocedurer og dokumentationssystemer, der sikrer produktkvalitet og patientsikkerhed.
Valideringskravene for farmaceutiske separationsteknologier omfatter omfattende test og dokumentation for at demonstrere, at udstyret konsekvent fremstiller produkter, der opfylder forudbestemte specifikationer. Denne proces omfatter faserne installationskvalificering, driftskvalificering og ydeevnekvalificering, som alle skal afsluttes, inden kommerciell drift kan påbegyndes.
Ændringskontrolprocedurer skal etableres for farmaceutiske separationsteknologier for at håndtere ændringer af driftsparametre, vedligeholdelsesprocedurer eller udstyrskonfigurationer. Disse procedurer sikrer, at alle ændringer vurderes, godkendes og dokumenteres korrekt for at opretholde regulatorisk overensstemmelse og produktkvalitet.
Dokumentations- og sporbarhedsstandarder
Farmaceutiske separationsteknologier kræver omfattende dokumentationssystemer, der registrerer udstyrets ydeevne, vedligeholdelsesaktiviteter og procesparametre gennem hele produktets levetid. Disse optegnelser skal opbevares i overensstemmelse med reguleringskravene og stilles til rådighed for inspektion af de pågældende myndigheder.
Sporbarehedskravene til farmaceutiske separationsteknologier omfatter opretholdelse af detaljerede optegnelser over råmaterialer, procesbetingelser og produktudgange for hver produktionsbatch. Denne information gør det muligt at foretage en hurtig undersøgelse af kvalitetsproblemer og understøtter eventuelle produkttilbagetrækningsprocedurer.
Elektroniske registreringssystemer, der anvendes sammen med farmaceutiske separationsteknologier, skal overholde reguleringskravene til dataintegritet, herunder bestemmelser om sikker lagring, kontrolleret adgang samt revisionsprotokoller, der sporer alle datamodifikationer eller -sletninger over tid.
Økonomiske og operationelle faktorer
Kapitalinvestering og driftsomkostninger
Den samlede ejerskabsomkostning for farmaceutiske separationsteknologier omfatter køb af udstyr, installationsomkostninger, løbende vedligeholdelsesomkostninger samt forbrug af energi og andre hjælpefunktioner gennem hele udstyrets levetid. Disse omkostninger skal vurderes i forhold til de forventede produktionsmængder og produktmargener for at fastslå den økonomiske levedygtighed.
Driftsomkostningerne for farmaceutiske separationsteknologier omfatter forbrugsartikler, energiforbrug, arbejdskraftsbehov samt omkostninger til affaldshåndtering. Energiforbedrede separationssystemer kan medføre betydelige besparelser over udstyrets levetid, især ved højkapacitetsdrift, hvor energiomkostningerne udgør en betydelig andel af de samlede driftsomkostninger.
Vedligeholdelsesomkostningerne for farmaceutiske separationsteknologier varierer betydeligt afhængigt af udstyrets kompleksitet, driftsmiljøet og vedligeholdelseskravene. Enkle mekaniske separationssystemer giver typisk lavere vedligeholdelsesomkostninger end komplekse kromatografiske eller kemiske separationssystemer, som kræver specialiseret teknisk support og udskiftelige komponenter.
Teknologiens levetid og risiko for forældelse
Den forventede levetid for farmaceutiske separationsteknologier bør vurderes i forhold til den forventede produktlevetid og den reguleringstekniske ramme. Teknologier med en lang levetid og et veletableret leverandørsupport giver større langtidsværdi og reducerer risikoen for forældelse under kritiske produktionsperioder.
Leverandørens stabilitet og tilgængelighed af teknisk support er afgørende faktorer ved valg af farmaceutiske separationsteknologier, da udstyrsproducenterne skal yde løbende support for reservedele, teknisk assistance og opdateringer af reguleringsmæssig overensstemmelse i hele udstyrets levetid.
Opgraderingsmuligheder for teknologien bør overvejes ved implementering af farmaceutiske separationsteknologier for at sikre, at udstyret kan modificeres eller forbedres, når produktionskravene ændrer sig eller nye reguleringsmæssige krav træder i kraft, uden at der kræves en fuldstændig udskiftning.
Implementerings- og optimeringsstrategier
Integration med eksisterende produktionssystemer
En vellykket implementering af farmaceutiske separationsteknologier kræver omhyggelig integration med den eksisterende produktionsinfrastruktur, herunder procesforløb før og efter separationen, hjælpeanlægssystemer og styresystemer. Denne integration sikrer en problemfri materialestrøm og optimal samlet proceseffektivitet, samtidig med at produktkvalitetsstandarderne opretholdes.
Kompatibilitet med styresystemer er afgørende, når farmaceutiske separationsteknologier integreres med eksisterende produktionsudstyr. Moderne separationssystemer bør levere standardiserede kommunikationsprotokoller og datagrænseflader, der muliggør problemfri integration med anlægsomspændende styre- og overvågningssystemer.
Kravene til operatørtræning for farmaceutiske separationsteknologier skal vurderes for at sikre, at der er tilstrækkelig ekspertise til rådighed for sikkert og effektivt udstyrsdrift. Træningsprogrammerne bør dække normal drift, fejlfinding, vedligeholdelsesprocedurer samt nødreaktionsprotokoller, der er specifikke for den valgte separationsteknologi.
Ydelsesovervågning og Optimering
Kontinuerlige overvågningssystemer for farmaceutiske separationsteknologier muliggør realtidsvurdering af separationens ydeevne og tidlig opdagelse af potentielle problemer, der kunne påvirke produktkvaliteten. Disse systemer bør registrere nøglepræstationsindikatorer såsom separationseffektivitet, gennemløbshastigheder og produktkvalitetsparametre.
Procesoptimering af farmaceutiske separationsteknologier omfatter en systematisk vurdering af driftsparametre for at maksimere separationsydelsen samtidig med, at driftsomkostningerne minimeres og overholdelse af reguleringskravene sikres. Denne optimering skal være baseret på statistisk designede eksperimenter og validerede analytiske metoder.
Regelmæssige ydelsesgennemgange af farmaceutiske separationsteknologier hjælper med at identificere muligheder for forbedring og sikrer fortsat overholdelse af de udviklede reguleringskrav. Disse gennemgange skal omfatte analyse af procesdata, vedligeholdelsesregistre og tendenser i produktkvaliteten for at understøtte initiativer til løbende forbedring.
Ofte stillede spørgsmål
Hvad er de mest kritiske faktorer ved valg af farmaceutiske separationsteknologier?
De mest kritiske faktorer omfatter krav til overholdelse af regler og forskrifter, specifikationer for produktrenhed, produktionsstørrelse samt den samlede ejerskabsomkostning. Den valgte teknologi skal opfylde kravene til god fremstillingspraksis (GMP), samtidig med at den opnår den krævede adskillelseseffektivitet og opretholder økonomisk levedygtighed for de påtænkte produktionsmængder.
Hvordan påvirker reguleringskravene udvælgelsen af farmaceutiske adskillelsteknologier?
Reguleringskravene kræver, at farmaceutiske adskillelsteknologier overholder retningslinjerne for god fremstillingspraksis (GMP), herunder udstyrsvalidering, dokumentationssystemer og procedurer for ændringskontrol. Disse krav foretrækker ofte etablerede teknologier med dokumenteret reguleringsmæssig accept og omfattende leverandørstøtte til valideringsaktiviteter.
Hvad er den typiske valideringstidslinje for implementering af nye farmaceutiske adskillelsteknologier?
Valideringstidsrammerne for farmaceutiske separationsteknologier ligger typisk mellem 6 og 18 måneder, afhængigt af udstyrets kompleksitet og regulatoriske krav. Denne tidsramme omfatter installationskvalificering, driftskvalificering, ydeevnekvalificering og procesvalideringsfaser, som alle skal gennemføres, inden der kan påbegyndes kommerciel produktion.
Hvordan vurderer du den langsigtet levedygtighed af farmaceutiske separationsteknologier?
Vurderingen af langsigtet levedygtighed tager hensyn til teknologiens modenhed, leverandørens stabilitet, vedligeholdelseskrav og regulatorisk accept. Teknologier med en velafprøvet historik, pålidelig leverandørstøtte og kompatibilitet med fremadrettede regulatoriske tendenser giver større langsigtet værdi og reducerer risikoen for forældelse i farmaceutiske produktionsoperationer.
Indholdsfortegnelse
- Forståelse af kategorier inden for farmaceutisk adskillelsteknologi
- Vurdering af proceskrav og specifikationer
- Regulering og overholdelsesovervejelser
- Økonomiske og operationelle faktorer
- Implementerings- og optimeringsstrategier
-
Ofte stillede spørgsmål
- Hvad er de mest kritiske faktorer ved valg af farmaceutiske separationsteknologier?
- Hvordan påvirker reguleringskravene udvælgelsen af farmaceutiske adskillelsteknologier?
- Hvad er den typiske valideringstidslinje for implementering af nye farmaceutiske adskillelsteknologier?
- Hvordan vurderer du den langsigtet levedygtighed af farmaceutiske separationsteknologier?