La scelta delle giuste tecnologie farmaceutiche di separazione è una decisione fondamentale che influisce direttamente sulla qualità del prodotto, sulla conformità normativa e sull’efficienza operativa nella produzione farmaceutica. Tale scelta richiede la valutazione di numerosi fattori, tra cui i composti specifici da trattare, i livelli di purezza richiesti, i volumi di produzione e i requisiti normativi che disciplinano i processi produttivi farmaceutici.

Il settore farmaceutico si basa su metodi di separazione precisi per garantire che i principi attivi farmaceutici rispettino rigorosi standard qualitativi, mantenendo al contempo convenienza economica e scalabilità. Comprendere il quadro decisionale relativo alle tecnologie di separazione farmaceutica consente ai produttori di ottimizzare i propri processi, ridurre i rischi di contaminazione e ottenere specifiche di prodotto costanti, conformi sia ai requisiti di approvazione regolatoria sia a quelli di fattibilità commerciale.
Comprensione delle categorie di tecnologie di separazione farmaceutica
Tecnologie di Separazione Meccanica
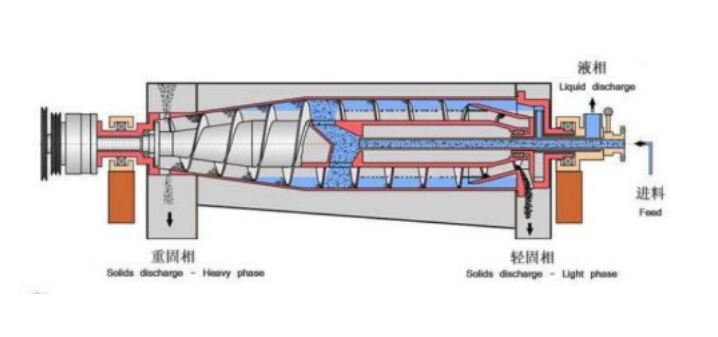
Le tecnologie meccaniche di separazione farmaceutica utilizzano forze fisiche per separare le particelle in base a differenze di dimensione, densità o forma. Questi metodi includono la centrifugazione, la filtrazione e i processi di setacciatura, che operano senza reazioni chimiche né cambiamenti di fase. I separatori centrifughi, in particolare i centrifughi decanter, si distinguono per l’eccellente capacità di separare le particelle solide dalla fase liquida nella produzione farmaceutica.
La scelta delle tecnologie meccaniche per la separazione farmaceutica dipende dalla distribuzione dimensionale delle particelle, dalle differenze di densità tra le fasi e dall’efficienza di separazione richiesta. Questi sistemi offrono vantaggi in termini di funzionamento continuo, scalabilità e minima contaminazione chimica, rendendoli adatti alla lavorazione di intermedi farmaceutici e prodotti finiti, dove il mantenimento dell’integrità chimica è di fondamentale importanza.
I metodi di separazione meccanica offrono inoltre un eccellente controllo sui parametri operativi, quali la forza centrifuga (G-force), il tempo di permanenza e le portate. Questo controllo consente ai produttori farmaceutici di ottimizzare le prestazioni di separazione mantenendo una qualità costante del prodotto e rispettando i requisiti normativi applicabili alle attrezzature per la lavorazione farmaceutica.
Metodi di separazione chimici e cromatografici
Gli approcci di separazione chimica nelle tecnologie farmaceutiche di separazione prevedono processi selettivi di dissoluzione, precipitazione o estrazione che sfruttano le differenze nelle proprietà chimiche tra i composti bersaglio e le impurità. Questi metodi offrono spesso una selettività superiore rispetto agli approcci meccanici, ma richiedono un’attenta valutazione della compatibilità chimica e dei requisiti di lavorazione a valle.
Le tecnologie farmaceutiche di separazione cromatografica offrono un’eccellente precisione per la purificazione dei principi attivi farmaceutici e la rimozione di impurità strettamente correlate. Questi sistemi utilizzano fasi stazionarie e mobili per ottenere una separazione selettiva basata sulle interazioni molecolari, anche se operano tipicamente in modalità batch e richiedono competenze specialistiche per l’ottimizzazione e la manutenzione.
La scelta tra metodi chimici e cromatografici dipende dai livelli di purezza richiesti, dalla scala di operazione e da considerazioni economiche. Sebbene queste tecnologie farmaceutiche di separazione possano raggiungere un’elevatissima selettività, spesso comportano costi operativi più elevati e un controllo del processo più complesso rispetto agli approcci meccanici di separazione.
Valutazione dei requisiti e delle specifiche del processo
Standard di qualità e purezza del prodotto
Le tecnologie farmaceutiche di separazione devono essere selezionate sulla base dei requisiti specifici di purezza stabiliti dagli standard farmacopeici e dalle autorità regolatorie. Il livello di purezza target influenza direttamente la complessità e il costo del sistema di separazione: requisiti di purezza più elevati richiedono tipicamente più stadi di separazione o tecnologie più sofisticate.
Comprendere la natura e la concentrazione delle impurità presenti nel materiale in ingresso è essenziale per scegliere le opportune tecnologie farmaceutiche di separazione. Alcune impurità potrebbero richiedere meccanismi di separazione specifici, mentre altre possono essere efficacemente rimosse utilizzando apparecchiature di separazione generiche, come centrifughe ad alta efficienza o sistemi avanzati di filtrazione.
Anche i metodi analitici utilizzati per verificare le prestazioni di separazione devono essere presi in considerazione nella scelta delle tecnologie farmaceutiche di separazione. Il sistema di separazione scelto deve produrre materiali che possano essere agevolmente analizzati mediante i comuni metodi di prova farmaceutica, rispettando al contempo le specifiche stabilite per identità, purezza e potenza.
Scala di produzione e requisiti di portata
I requisiti relativi al volume di produzione influenzano in modo significativo la scelta delle tecnologie farmaceutiche di separazione, poiché diverse tecnologie presentano caratteristiche di scalabilità e capacità di throughput differenti. Le separazioni su piccola scala in laboratorio possono ricorrere ad approcci diversi rispetto alla produzione commerciale su larga scala, richiedendo un’attenta valutazione della fattibilità della scala-up.
Anche la preferenza per il funzionamento continuo rispetto a quello discontinuo influenza la scelta delle tecnologie farmaceutiche di separazione. I sistemi di separazione continua, come tecnologie di separazione farmaceutica quelli che utilizzano centrifughe decanter, offrono vantaggi per la produzione ad alto volume, mentre i sistemi discontinui possono garantire un maggiore controllo per prodotti specializzati o ad alto valore.
La flessibilità nel gestire composizioni variabili del materiale in ingresso e piani di produzione deve essere valutata nella scelta delle tecnologie farmaceutiche di separazione. I sistemi in grado di adattarsi a variazioni nelle caratteristiche del materiale in ingresso o alle esigenze produttive offrono vantaggi operativi e contribuiscono all’ottimizzazione dell’efficienza complessiva della produzione.
Considerazioni normative e di conformità
Requisiti di Buone Pratiche di Produzione
Tutte le tecnologie farmaceutiche di separazione devono rispettare le linee guida delle Buone Prassi di Fabbricazione (GMP), che disciplinano la progettazione, l’uso e la manutenzione degli impianti nelle strutture produttive farmaceutiche. Tali requisiti comprendono specifiche relative ai materiali costitutivi, alle finiture superficiali, alle procedure di pulizia e ai sistemi di documentazione, al fine di garantire la qualità del prodotto e la sicurezza del paziente.
I requisiti di convalida per le tecnologie farmaceutiche di separazione prevedono test e documentazione completi per dimostrare che le attrezzature producono in modo costante prodotti conformi alle specifiche predeterminate. Questo processo comprende le fasi di qualifica d’installazione, qualifica funzionale e qualifica prestazionale, che devono essere completate prima dell’avvio dell’attività commerciale.
Devono essere istituite procedure di controllo delle modifiche per le tecnologie farmaceutiche di separazione, al fine di gestire le variazioni dei parametri operativi, delle procedure di manutenzione o delle configurazioni degli impianti. Tali procedure garantiscono che ogni modifica venga adeguatamente valutata, approvata e documentata per mantenere la conformità normativa e la qualità del prodotto.
Standard di Documentazione e Tracciabilità
Le tecnologie farmaceutiche di separazione richiedono sistemi documentali completi che registrino le prestazioni degli impianti, le attività di manutenzione e i parametri di processo durante l'intero ciclo di vita del prodotto. Questi registri devono essere conservati nel rispetto dei requisiti normativi e resi disponibili per ispezione da parte delle autorità regolatorie.
I requisiti di tracciabilità per le tecnologie farmaceutiche di separazione comprendono la conservazione di registri dettagliati relativi ai materiali in ingresso, alle condizioni di processo e agli output produttivi per ogni lotto di produzione. Queste informazioni consentono un'indagine rapida su eventuali problemi di qualità e supportano le procedure di ritiro del prodotto, se necessario.
I sistemi di registrazione elettronica utilizzati con le tecnologie farmaceutiche di separazione devono conformarsi ai requisiti normativi in materia di integrità dei dati, comprese le disposizioni relative alla memorizzazione sicura, all'accesso controllato e ai registri di audit che traccino tutte le modifiche o cancellazioni dei dati nel tempo.
Fattori Economici e Operativi
Investimento in Capitale e Costi Operativi
Il costo totale di proprietà delle tecnologie farmaceutiche di separazione comprende l'acquisto iniziale dell'attrezzatura, i costi di installazione, le spese di manutenzione continua e il consumo di servizi ausiliari durante tutto il ciclo di vita dell'attrezzatura. Questi costi devono essere valutati in relazione ai volumi di produzione previsti e ai margini di prodotto per determinarne la convenienza economica.
I costi operativi delle tecnologie farmaceutiche di separazione comprendono i materiali di consumo, il consumo energetico, le esigenze di manodopera e le spese per lo smaltimento dei rifiuti. I sistemi di separazione ad alta efficienza energetica possono generare significativi risparmi sui costi nel corso della vita utile dell'attrezzatura, in particolare nelle operazioni ad alto throughput, dove i costi relativi ai servizi ausiliari rappresentano una quota consistente delle spese operative.
I costi di manutenzione per le tecnologie di separazione farmaceutica variano notevolmente in base alla complessità dell’attrezzatura, all’ambiente operativo e ai requisiti di manutenzione. I sistemi di separazione meccanica semplici offrono generalmente costi di manutenzione inferiori rispetto ai sistemi di separazione cromatografici o chimici complessi, che richiedono un supporto tecnico specializzato e componenti di ricambio.
Ciclo di vita della tecnologia e rischio di obsolescenza
La durata prevista di servizio delle tecnologie di separazione farmaceutica deve essere valutata in relazione al ciclo di vita previsto del prodotto e al contesto normativo. Le tecnologie con una lunga durata di servizio e un consolidato supporto da parte dei fornitori offrono un maggiore valore a lungo termine e riducono il rischio di obsolescenza durante periodi critici di produzione.
La stabilità dei fornitori e la disponibilità del supporto tecnico sono fattori cruciali nella selezione delle tecnologie farmaceutiche per la separazione, poiché i produttori di apparecchiature devono garantire un supporto continuativo per ricambi, assistenza tecnica e aggiornamenti relativi alla conformità normativa durante l’intero ciclo di vita delle apparecchiature.
È opportuno considerare i percorsi di aggiornamento tecnologico nell’implementazione delle tecnologie farmaceutiche per la separazione, al fine di assicurare che le apparecchiature possano essere modificate o potenziate in risposta all’evoluzione dei requisiti produttivi o all’introduzione di nuovi obblighi normativi, senza dover procedere a una sostituzione completa.
Strategie di Implementazione e Ottimizzazione
Integrazione con i sistemi produttivi esistenti
L’implementazione con successo delle tecnologie farmaceutiche per la separazione richiede un’attenta integrazione con le infrastrutture produttive esistenti, compresi i processi a monte e a valle, i sistemi di servizi ausiliari e i sistemi di controllo. Tale integrazione garantisce un flusso di materiali regolare e un’efficienza complessiva ottimale del processo, preservando nel contempo gli standard di qualità del prodotto.
La compatibilità del sistema di controllo è essenziale quando si integrano le tecnologie farmaceutiche di separazione con le attrezzature di produzione esistenti. I sistemi moderni di separazione devono fornire protocolli di comunicazione standardizzati e interfacce dati che consentano un’integrazione senza soluzione di continuità con i sistemi di controllo e monitoraggio a livello di impianto.
I requisiti formativi per gli operatori relativi alle tecnologie farmaceutiche di separazione devono essere valutati per garantire la disponibilità di competenze adeguate per un funzionamento sicuro ed efficace delle attrezzature. I programmi di formazione devono coprire il funzionamento normale, la risoluzione dei guasti, le procedure di manutenzione e i protocolli di risposta alle emergenze specifici della tecnologia di separazione scelta.
Monitoraggio e Ottimizzazione delle Prestazioni
I sistemi di monitoraggio continuo per le tecnologie farmaceutiche di separazione consentono una valutazione in tempo reale delle prestazioni di separazione e un rilevamento precoce di potenziali problemi che potrebbero influenzare la qualità del prodotto. Tali sistemi devono rilevare indicatori chiave di prestazione, quali l’efficienza di separazione, le portate di processo e i parametri di qualità del prodotto.
L'ottimizzazione del processo per le tecnologie farmaceutiche di separazione prevede una valutazione sistematica dei parametri operativi al fine di massimizzare le prestazioni di separazione, riducendo al contempo i costi operativi e garantendo la conformità ai requisiti normativi.
I regolari controlli delle prestazioni delle tecnologie farmaceutiche di separazione consentono di individuare opportunità di miglioramento e di assicurare il rispetto continuo dei requisiti normativi in evoluzione. Tali controlli devono includere l’analisi dei dati di processo, dei registri di manutenzione e delle tendenze relative alla qualità del prodotto, al fine di supportare le iniziative di miglioramento continuo.
Domande frequenti
Quali sono i fattori più critici nella scelta delle tecnologie farmaceutiche di separazione?
I fattori più critici includono i requisiti di conformità normativa, le specifiche di purezza del prodotto, la scala di produzione e il costo totale di proprietà. La tecnologia selezionata deve rispettare gli standard delle Buone Pratiche di Produzione (GMP), garantendo al contempo l’efficienza di separazione richiesta e la sostenibilità economica per i volumi di produzione previsti.
In che modo i requisiti normativi influenzano la scelta delle tecnologie farmaceutiche di separazione?
I requisiti normativi stabiliscono che le tecnologie farmaceutiche di separazione devono conformarsi alle linee guida delle Buone Pratiche di Produzione (GMP), comprese la convalida degli impianti, i sistemi di documentazione e le procedure di controllo delle modifiche. Tali requisiti favoriscono spesso tecnologie consolidate, già riconosciute a livello normativo e supportate da fornitori in grado di offrire un’assistenza completa per le attività di convalida.
Qual è il tempo tipico necessario per la convalida dell’implementazione di nuove tecnologie farmaceutiche di separazione?
I tempi necessari per la convalida delle tecnologie farmaceutiche di separazione variano tipicamente da 6 a 18 mesi, in base alla complessità dell’attrezzatura e ai requisiti normativi. Questo cronoprogramma comprende le fasi di qualifica d’installazione, qualifica operativa, qualifica prestazionale e convalida del processo, che devono essere completate prima dell’avvio della produzione commerciale.
Come si valuta la sostenibilità a lungo termine delle tecnologie farmaceutiche di separazione?
La valutazione della sostenibilità a lungo termine tiene conto della maturità tecnologica, della stabilità del fornitore, dei requisiti di manutenzione e dell’accettazione normativa. Le tecnologie con un consolidato track record, un supporto affidabile da parte dei fornitori e una compatibilità con le tendenze normative emergenti offrono un maggiore valore a lungo termine e riducono il rischio di obsolescenza nelle operazioni di produzione farmaceutica.
Indice
- Comprensione delle categorie di tecnologie di separazione farmaceutica
- Valutazione dei requisiti e delle specifiche del processo
- Considerazioni normative e di conformità
- Fattori Economici e Operativi
- Strategie di Implementazione e Ottimizzazione
-
Domande frequenti
- Quali sono i fattori più critici nella scelta delle tecnologie farmaceutiche di separazione?
- In che modo i requisiti normativi influenzano la scelta delle tecnologie farmaceutiche di separazione?
- Qual è il tempo tipico necessario per la convalida dell’implementazione di nuove tecnologie farmaceutiche di separazione?
- Come si valuta la sostenibilità a lungo termine delle tecnologie farmaceutiche di separazione?