Wybór odpowiednich technologii separacji farmaceutycznej to kluczowa decyzja, która bezpośrednio wpływa na jakość produktu, zgodność z przepisami i wydajność operacyjną w produkcji farmaceutycznej. Wybór ten wymaga oceny wielu czynników, w tym konkretnych przetwarzanych związków, wymaganych poziomów czystości, wielkości produkcji oraz wymogów regulacyjnych regulujących procesy produkcji farmaceutycznej.

Przemysł farmaceutyczny polega na precyzyjnych metodach rozdzielania, aby zapewnić, że substancje czynne spełniają surowe wymagania jakościowe, zachowując przy tym opłacalność i skalowalność. Zrozumienie ram decyzyjnych dotyczących technologii rozdzielania w przemyśle farmaceutycznym umożliwia producentom zoptymalizowanie swoich procesów, zmniejszenie ryzyka zanieczyszczenia oraz osiągnięcie spójnych specyfikacji produktu, które spełniają zarówno wymagania regulacyjne, jak i warunki opłacalności komercyjnej.
Zrozumienie kategorii technologii rozdzielania w przemyśle farmaceutycznym
Technologie Mechanicznej Separacji
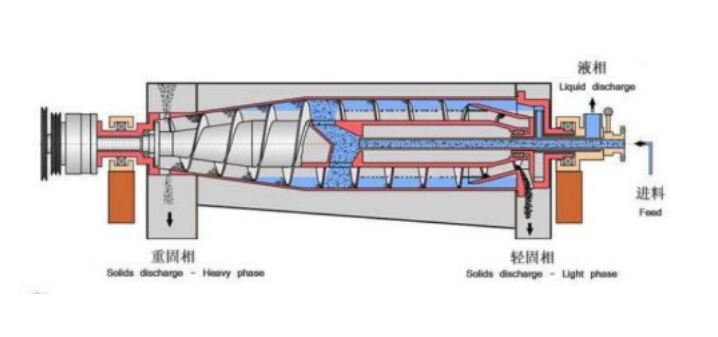
Mechaniczne technologie rozdzielania farmaceutycznego wykorzystują siły fizyczne do oddzielania cząstek na podstawie różnic ich wielkości, gęstości lub kształtu. Do metod tych należą m.in. wirowanie, filtracja oraz procesy sitowania, które przebiegają bez udziału reakcji chemicznych lub zmian fazowych. Separatory odśrodkowe, w szczególności separatory odśrodkowe typu dekanter, doskonale sprawdzają się w oddzielaniu cząstek stałych od fazy ciekłej w produkcji farmaceutycznej.
Wybór mechanicznych technologii rozdziału farmaceutycznego zależy od rozkładu wielkości cząstek, różnic gęstości między fazami oraz wymaganej wydajności rozdziału. Te systemy oferują zalety związane z ciągłą pracą, skalowalnością oraz minimalnym zanieczyszczeniem chemicznym, co czyni je odpowiednimi do przetwarzania pośrednich produktów farmaceutycznych i gotowych leków, gdzie zachowanie integralności chemicznej jest kluczowe.
Metody rozdziału mechanicznego zapewniają również doskonałą kontrolę parametrów pracy, takich jak siła odśrodkowa (G), czas przebywania materiału w urządzeniu oraz szybkość przepływu. Dzięki tej kontroli producenci farmaceutyczni mogą zoptymalizować wydajność rozdziału, zachowując przy tym stałą jakość produktu oraz spełniając wymagania regulacyjne dotyczące sprzętu stosowanego w przetwarzaniu farmaceutycznym.
Metody rozdziału chemicznego i chromatograficznego
Metody chemicznej separacji w technologiach separacji farmaceutycznych obejmują selektywne rozpuszczanie, strącanie lub ekstrakcję, wykorzystujące różnice w właściwościach chemicznych między związkami docelowymi a zanieczyszczeniami. Metody te często zapewniają wyższą selektywność niż podejścia mechaniczne, ale wymagają starannego uwzględnienia zgodności chemicznej oraz wymagań związanych z przetwarzaniem w dalszych etapach.
Chromatograficzne technologie separacji farmaceutycznej oferują wyjątkową precyzję w oczyszczaniu czynnych składników farmaceutycznych oraz usuwaniu blisko spokrewnionych zanieczyszczeń. W systemach tych wykorzystuje się fazę nieruchomą i fazę ruchomą w celu osiągnięcia selektywnej separacji na podstawie oddziaływań molekularnych, choć zwykle działają one w trybie partii i wymagają wyspecjalizowanej wiedzy do ich optymalizacji oraz konserwacji.
Wybór między metodami chemicznymi a chromatograficznymi zależy od wymaganych poziomów czystości, skali działania oraz uwarunkowań ekonomicznych. Choć te technologie rozdzielania stosowane w przemyśle farmaceutycznym pozwalają osiągnąć bardzo wysoką selektywność, często wiążą się one z wyższymi kosztami eksploatacji oraz bardziej złożoną kontrolą procesu w porównaniu do podejść opartych na rozdzielaniu mechanicznym.
Ocena wymagań i specyfikacji procesu
Standardy jakości i czystości produktu
Technologie rozdzielania stosowane w przemyśle farmaceutycznym należy dobierać na podstawie konkretnych wymagań dotyczących czystości określonych w standardach farmakopealnych oraz przez organy regulacyjne. Poziom docelowej czystości ma bezpośredni wpływ na złożoność i koszty systemu rozdzielania; wyższe wymagania dotyczące czystości zwykle wymagają zastosowania wielu etapów rozdzielania lub bardziej zaawansowanych technologii.
Zrozumienie natury i stężenia zanieczyszczeń obecnych w materiale wejściowym jest kluczowe przy wyborze odpowiednich technologii separacji farmaceutycznej. Niektóre zanieczyszczenia mogą wymagać specyficznych mechanizmów separacji, podczas gdy inne można skutecznie usunąć za pomocą uniwersalnego sprzętu do separacji, takiego jak wysokowydajne wirówki lub zaawansowane systemy filtracji.
Przy wyborze technologii separacji farmaceutycznej należy również wziąć pod uwagę metody analityczne stosowane do weryfikacji skuteczności separacji. Wybrany system separacji powinien generować produkty, które można łatwo analizować za pomocą standardowych metod badawczych stosowanych w przemyśle farmaceutycznym, jednocześnie spełniając ustalone specyfikacje dotyczące tożsamości, czystości i aktywności.
Skala produkcji oraz wymagania dotyczące wydajności
Wymagania dotyczące objętości produkcji znacząco wpływają na wybór technologii rozdzielania farmaceutycznego, ponieważ różne technologie charakteryzują się różnymi cechami skalowalności oraz możliwościami przepustowości. Rozdzielenia w małej skali laboratoryjnej mogą wykorzystywać inne podejścia niż produkcja komercyjna w dużej skali, co wymaga starannego rozważenia możliwości skalowania w górę.
Preferencje dotyczące pracy ciągłej lub partii również wpływają na wybór technologii rozdzielania farmaceutycznego. Systemy rozdzielania ciągłego, takie jak technologie separacji w przemyśle farmaceutycznym wykorzystujące wirówki odśrodkowe typu decanter, oferują zalety w przypadku produkcji o wysokiej objętości, podczas gdy systemy partii mogą zapewniać lepszą kontrolę w przypadku produktów specjalistycznych lub o wysokiej wartości.
Elastyczność w obsłudze zmiennych składów surowca i harmonogramów produkcji powinna zostać oceniona przy wyborze technologii rozdzielania stosowanych w przemyśle farmaceutycznym. Systemy, które mogą dostosować się do zmian w charakterystyce surowca lub wymogach produkcyjnych, zapewniają korzyści operacyjne oraz wspierają optymalizację ogólnej wydajności procesu produkcyjnego.
Uwagi prawne i dotyczące zgodności
Wymagania GMP
Wszystkie technologie rozdzielania stosowane w przemyśle farmaceutycznym muszą być zgodne z wytycznymi Dobrych Praktyk Produkcyjnych (GMP), regulującymi projektowanie, eksploatację i konserwację sprzętu w zakładach produkcyjnych wyrobów farmaceutycznych. Wymagania te obejmują specyfikacje dotyczące materiałów konstrukcyjnych, jakości powierzchni, procedur czyszczenia oraz systemów dokumentacji, które zapewniają jakość produktu i bezpieczeństwo pacjentów.
Wymagania dotyczące walidacji technologii rozdzielania w przemyśle farmaceutycznym obejmują kompleksowe badania i dokumentację mające na celu wykazanie, że sprzęt w sposób ciągły wytwarza produkty spełniające ustalone specyfikacje. Proces ten obejmuje etapy kwalifikacji instalacyjnej, kwalifikacji eksploatacyjnej oraz kwalifikacji wydajnościowej, które muszą zostać ukończone przed rozpoczęciem działalności komercyjnej.
Dla technologii rozdzielania w przemyśle farmaceutycznym należy opracować procedury kontroli zmian w celu zarządzania modyfikacjami parametrów eksploatacyjnych, procedur konserwacji lub konfiguracji sprzętu. Procedury te zapewniają, że wszystkie zmiany są odpowiednio oceniane, zatwierdzane i udokumentowane, co umożliwia zachowanie zgodności z wymaganiami regulacyjnymi oraz jakości produktów.
Standardy dokumentacji i śledzenia
Technologie rozdzielania farmaceutycznego wymagają kompleksowych systemów dokumentacji śledzących wydajność sprzętu, działania serwisowe oraz parametry procesu w całym cyklu życia produktu. Rejestry te muszą być prowadzone zgodnie z wymaganiami regulacyjnymi i udostępniane organom nadzorującym na żądanie.
Wymagania dotyczące śledzenia w zakresie technologii rozdzielania farmaceutycznego obejmują prowadzenie szczegółowych rejestrów materiałów wejściowych, warunków przetwarzania oraz wyjść produktu dla każdej partii produkcyjnej. Informacje te umożliwiają szybkie wyjaśnienie problemów jakościowych oraz wspierają procedury wycofywania produktu w razie konieczności.
Systemy rejestracji elektronicznej stosowane w połączeniu z technologiami rozdzielania farmaceutycznego muszą spełniać wymagania regulacyjne dotyczące integralności danych, w tym przepisy dotyczące bezpiecznego przechowywania, kontrolowanego dostępu oraz śladów audytowych śledzących wszystkie modyfikacje lub usunięcia danych w czasie.
Czynniki ekonomiczne i operacyjne
Inwestycje kapitałowe i koszty operacyjne
Całkowity koszt posiadania technologii rozdzielania w przemyśle farmaceutycznym obejmuje zakup początkowy sprzętu, koszty instalacji, bieżące wydatki na konserwację oraz zużycie mediów energetycznych w całym okresie użytkowania sprzętu. Koszty te należy ocenić w odniesieniu do prognozowanych objętości produkcji oraz marż z produktów, aby określić opłacalność ekonomiczną.
Koszty eksploatacji technologii rozdzielania w przemyśle farmaceutycznym obejmują zużywane materiały eksploatacyjne, zużycie energii, zapotrzebowanie na siłę roboczą oraz koszty utylizacji odpadów. Energooszczędne systemy rozdzielania mogą przynieść znaczne oszczędności w całym okresie użytkowania sprzętu, szczególnie w przypadku operacji o wysokiej wydajności, gdzie koszty mediów energetycznych stanowią istotną część kosztów operacyjnych.
Koszty konserwacji technologii rozdzielania stosowanych w przemyśle farmaceutycznym różnią się znacznie w zależności od złożoności sprzętu, warunków eksploatacji oraz wymagań dotyczących konserwacji. Proste mechaniczne systemy rozdzielania charakteryzują się zwykle niższymi kosztami konserwacji w porównaniu do złożonych systemów chromatograficznych lub chemicznych, które wymagają specjalistycznej obsługi technicznej oraz wymiany komponentów.
Cykl życia technologii i ryzyko przestarzałości
Oczekiwany okres użytkowania technologii rozdzielania stosowanych w przemyśle farmaceutycznym należy ocenić w odniesieniu do przewidywanego cyklu życia produktu oraz obowiązującego środowiska regulacyjnego. Technologie o długim okresie użytkowania oraz zapewnionej przez dostawców wsparcie zapewniają wyższą wartość długoterminową oraz zmniejszają ryzyko przestarzałości w kluczowych okresach produkcji.
Stabilność dostawcy i dostępność wsparcia technicznego są kluczowymi czynnikami przy wyborze technologii separacji farmaceutycznej, ponieważ producenci sprzętu muszą zapewniać ciągłe wsparcie w zakresie części zamiennych, pomocy technicznej oraz aktualizacji dotyczących zgodności z przepisami na całym etapie eksploatacji sprzętu.
Przy wdrażaniu technologii separacji farmaceutycznej należy uwzględnić ścieżki uaktualniania technologii, aby zapewnić możliwość modyfikacji lub ulepszania sprzętu w miarę zmian wymagań produkcyjnych lub wprowadzania nowych wymogów regulacyjnych bez konieczności pełnej jego wymiany.
Strategie wdrażania i optymalizacji
Integracja z istniejącymi systemami produkcyjnymi
Pomyślne wdrożenie technologii separacji farmaceutycznej wymaga starannego zintegrowania ich z istniejącą infrastrukturą produkcyjną, w tym z procesami poprzedzającymi i następującymi po nich, systemami pomocniczymi oraz systemami sterowania. Takie zintegrowanie zapewnia płynny przepływ materiałów i optymalną ogólną wydajność procesu, zachowując jednocześnie standardy jakości produktu.
Zgodność systemu sterowania jest kluczowa przy integracji technologii rozdzielania farmaceutycznego z istniejącym wyposażeniem produkcyjnym. Nowoczesne systemy rozdzielania powinny zapewniać standaryzowane protokoły komunikacyjne oraz interfejsy danych umożliwiające bezproblemową integrację z systemami kontroli i monitoringu obejmującymi całą zakład produkcyjny.
Wymagania szkoleniowe dla operatorów w zakresie technologii rozdzielania farmaceutycznego należy ocenić, aby zapewnić dostępność odpowiedniej wiedzy i umiejętności niezbędnych do bezpiecznej i skutecznej obsługi sprzętu. Programy szkoleniowe powinny obejmować obsługę w warunkach normalnych, diagnozowanie i usuwanie awarii, procedury konserwacji oraz protokoły postępowania w sytuacjach nagłych, specyficzne dla wybranej technologii rozdzielania.
Monitorowanie i optymalizacja wydajności
Systemy ciągłego monitoringu technologii rozdzielania farmaceutycznego umożliwiają ocenę w czasie rzeczywistym skuteczności procesu rozdzielania oraz wczesne wykrywanie potencjalnych problemów, które mogłyby wpłynąć na jakość produktu. Takie systemy powinny śledzić kluczowe wskaźniki wydajności, takie jak skuteczność rozdzielania, szybkość przepływu (throughput) oraz parametry jakości produktu.
Optymalizacja procesów w technologiach rozdzielania stosowanych w przemyśle farmaceutycznym obejmuje systematyczną ocenę parametrów eksploatacyjnych w celu maksymalizacji wydajności rozdzielania przy jednoczesnym minimalizowaniu kosztów eksploatacji i zapewnieniu zgodności z wymaganiami regulacyjnymi.
Regularne przeglądy wydajności technologii rozdzielania stosowanych w przemyśle farmaceutycznym pomagają zidentyfikować możliwości poprawy oraz zapewniają utrzymanie zgodności z dynamicznie zmieniającymi się wymaganiami regulacyjnymi. Przeglądy te powinny obejmować analizę danych procesowych, dokumentacji konserwacji oraz trendów jakości produktów w celu wspierania inicjatyw ciągłej poprawy.
Często zadawane pytania
Jakie są najważniejsze czynniki decydujące o wyborze technologii rozdzielania stosowanych w przemyśle farmaceutycznym?
Najważniejszymi czynnikami są wymagania dotyczące zgodności z przepisami, specyfikacje czystości produktu, skala produkcji oraz całkowity koszt posiadania. Wybrana technologia musi spełniać standardy Dobrej Praktyki Produkcyjnej (GMP), osiągając wymaganą wydajność rozdziału i zapewniając opłacalność ekonomiczną przy planowanych objętościach produkcji.
W jaki sposób wymagania regulacyjne wpływają na wybór technologii rozdziału w przemyśle farmaceutycznym?
Wymagania regulacyjne nakazują, aby technologie rozdziału stosowane w przemyśle farmaceutycznym były zgodne z wytycznymi Dobrej Praktyki Produkcyjnej (GMP), w tym z walidacją urządzeń, systemami dokumentacji oraz procedurami kontroli zmian. Wymagania te często sprzyjają sprawdzonym technologiom, które mają potwierdzoną akceptację regulacyjną oraz kompleksową pomoc dostawców w zakresie działań walidacyjnych.
Jaki jest typowy czas trwania procesu walidacji przy wdrażaniu nowych technologii rozdziału w przemyśle farmaceutycznym?
Czas trwania walidacji technologii separacyjnych w przemyśle farmaceutycznym zwykle wynosi od 6 do 18 miesięcy i zależy od złożoności sprzętu oraz wymogów regulacyjnych. Czas ten obejmuje etapy kwalifikacji instalacji, kwalifikacji eksploatacyjnej, kwalifikacji wydajnościowej oraz walidacji procesu, które muszą zostać ukończone przed rozpoczęciem produkcji komercyjnej.
W jaki sposób ocenia się długoterminową żywotność technologii separacyjnych w przemyśle farmaceutycznym?
Ocena długoterminowej żywotności uwzględnia dojrzałość technologii, stabilność dostawcy, wymagania serwisowe oraz akceptację regulacyjną. Technologie o sprawdzonej historii stosowania, niezawodnym wsparciu ze strony dostawcy oraz zgodności z nowymi trendami regulacyjnymi zapewniają wyższą wartość długoterminową oraz niższe ryzyko przestarzenia w operacjach produkcyjnych w przemyśle farmaceutycznym.
Spis treści
- Zrozumienie kategorii technologii rozdzielania w przemyśle farmaceutycznym
- Ocena wymagań i specyfikacji procesu
- Uwagi prawne i dotyczące zgodności
- Czynniki ekonomiczne i operacyjne
- Strategie wdrażania i optymalizacji
-
Często zadawane pytania
- Jakie są najważniejsze czynniki decydujące o wyborze technologii rozdzielania stosowanych w przemyśle farmaceutycznym?
- W jaki sposób wymagania regulacyjne wpływają na wybór technologii rozdziału w przemyśle farmaceutycznym?
- Jaki jest typowy czas trwania procesu walidacji przy wdrażaniu nowych technologii rozdziału w przemyśle farmaceutycznym?
- W jaki sposób ocenia się długoterminową żywotność technologii separacyjnych w przemyśle farmaceutycznym?