Selecionar as tecnologias certas de separação farmacêutica é uma decisão crítica que afeta diretamente a qualidade do produto, a conformidade regulatória e a eficiência operacional na fabricação farmacêutica. Essa escolha envolve a avaliação de diversos fatores, incluindo os compostos específicos a serem processados, os níveis de pureza exigidos, os volumes de produção e os requisitos regulatórios que regem os processos de fabricação farmacêutica.

A indústria farmacêutica depende de métodos precisos de separação para garantir que os princípios ativos farmacêuticos atendam a rigorosos padrões de qualidade, mantendo ao mesmo tempo a rentabilidade e a escalabilidade. Compreender o quadro decisório para as tecnologias de separação farmacêutica permite que os fabricantes otimizem seus processos, reduzam os riscos de contaminação e alcancem especificações de produto consistentes, atendendo tanto aos requisitos de aprovação regulatória quanto à viabilidade comercial.
Compreensão das Categorias de Tecnologias de Separação Farmacêutica
Tecnologias de Separação Mecânica
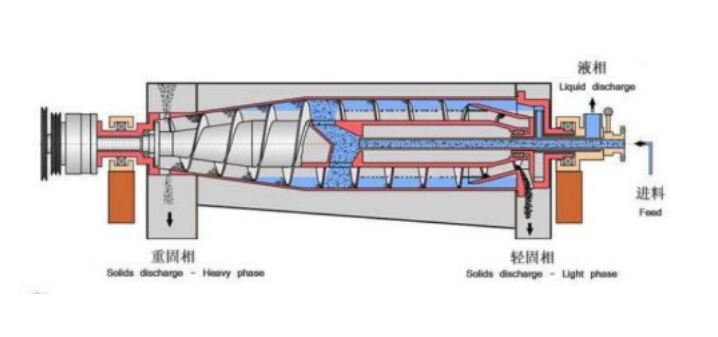
As tecnologias mecânicas de separação farmacêutica utilizam forças físicas para separar partículas com base em diferenças de tamanho, densidade ou forma. Esses métodos incluem centrifugação, filtração e processos de peneiramento que operam sem reações químicas ou mudanças de fase. Os separadores centrífugos, especialmente as centrífugas decantadoras, destacam-se na separação de partículas sólidas da fase líquida na fabricação farmacêutica.
A seleção das tecnologias mecânicas de separação farmacêutica depende da distribuição do tamanho das partículas, das diferenças de densidade entre as fases e da eficiência de separação exigida. Esses sistemas oferecem vantagens em termos de operação contínua, escalabilidade e contaminação química mínima, tornando-os adequados para o processamento de intermedários farmacêuticos e produtos finais, onde a manutenção da integridade química é fundamental.
Os métodos mecânicos de separação também proporcionam excelente controle sobre parâmetros operacionais, como força G, tempo de residência e taxas de vazão. Esse controle permite que os fabricantes farmacêuticos otimizem o desempenho da separação, mantendo a qualidade consistente do produto e atendendo aos requisitos regulatórios para equipamentos de processamento farmacêutico.
Métodos Químicos e Cromatográficos de Separação
As abordagens químicas de separação nas tecnologias farmacêuticas de separação envolvem processos seletivos de dissolução, precipitação ou extração que exploram as diferenças nas propriedades químicas entre os compostos-alvo e as impurezas. Esses métodos frequentemente oferecem maior seletividade do que as abordagens mecânicas, mas exigem uma avaliação cuidadosa da compatibilidade química e dos requisitos de processamento posterior.
As tecnologias cromatográficas de separação farmacêutica oferecem precisão excepcional para a purificação de princípios ativos farmacêuticos e a remoção de impurezas estruturalmente semelhantes. Esses sistemas utilizam fases estacionária e móvel para alcançar separação seletiva com base em interações moleculares, embora normalmente operem em modo descontínuo (batch) e exijam conhecimento especializado para otimização e manutenção.
A escolha entre métodos químicos e cromatográficos depende dos níveis de pureza exigidos, da escala de operação e de considerações econômicas. Embora essas tecnologias de separação farmacêutica possam atingir alta seletividade, frequentemente envolvem custos operacionais mais elevados e controle de processo mais complexo, comparados às abordagens mecânicas de separação.
Avaliação dos Requisitos e Especificações do Processo
Padrões de Qualidade e Pureza do Produto
As tecnologias farmacêuticas de separação devem ser selecionadas com base nos requisitos específicos de pureza estabelecidos pelas normas farmacopeicas e pelas autoridades regulatórias. O nível de pureza alvo influencia diretamente a complexidade e o custo do sistema de separação, sendo que requisitos mais elevados de pureza normalmente exigem múltiplos estágios de separação ou tecnologias mais sofisticadas.
Compreender a natureza e a concentração das impurezas presentes no material de alimentação é essencial para a escolha das tecnologias farmacêuticas de separação adequadas. Algumas impurezas podem exigir mecanismos específicos de separação, enquanto outras podem ser removidas eficazmente com equipamentos de separação de uso geral, como centrífugas de alta eficiência ou sistemas avançados de filtração.
Os métodos analíticos utilizados para verificar o desempenho de separação também devem ser considerados ao selecionar tecnologias farmacêuticas de separação. O sistema de separação escolhido deve produzir produtos que possam ser facilmente analisados utilizando métodos padrão de ensaio farmacêutico, ao mesmo tempo em que atendem às especificações estabelecidas quanto à identidade, pureza e potência.
Escala de Produção e Requisitos de Capacidade de Processamento
Os requisitos de volume de produção influenciam significativamente a seleção de tecnologias farmacêuticas de separação, uma vez que diferentes tecnologias apresentam características variáveis de escalabilidade e capacidades de throughput. Separações em laboratório em pequena escala podem empregar abordagens distintas das utilizadas na produção comercial em larga escala, exigindo uma avaliação cuidadosa da viabilidade da ampliação de escala.
As preferências por operação contínua ou em batelada também afetam a escolha das tecnologias farmacêuticas de separação. Sistemas de separação contínua, tais como tecnologias de separação farmacêutica utilizando centrífugas decantadoras, oferecem vantagens para produção em grande volume, enquanto sistemas descontínuos podem proporcionar melhor controle para produtos especializados ou de alto valor.
A flexibilidade para lidar com composições variáveis da alimentação e com cronogramas de produção deve ser avaliada ao selecionar tecnologias farmacêuticas de separação. Sistemas capazes de acomodar alterações nas características da alimentação ou nas demandas de produção proporcionam vantagens operacionais e ajudam a otimizar a eficiência geral da fabricação.
Considerações Regulatórias e de Conformidade
Requisitos de Boas Práticas de Fabricação
Todas as tecnologias farmacêuticas de separação devem estar em conformidade com as diretrizes das Boas Práticas de Fabricação que regulamentam o projeto, a operação e a manutenção de equipamentos nas instalações farmacêuticas. Esses requisitos incluem especificações quanto aos materiais de construção, acabamentos superficiais, procedimentos de limpeza e sistemas de documentação que garantam a qualidade do produto e a segurança do paciente.
Os requisitos de validação para tecnologias farmacêuticas de separação envolvem testes e documentação abrangentes para demonstrar que o equipamento produz consistentemente produtos que atendem às especificações predeterminadas. Esse processo inclui as fases de qualificação de instalação, qualificação operacional e qualificação de desempenho, que devem ser concluídas antes da operação comercial.
Devem ser estabelecidos procedimentos de controle de mudanças para tecnologias farmacêuticas de separação, a fim de gerenciar modificações nos parâmetros operacionais, nos procedimentos de manutenção ou nas configurações do equipamento. Esses procedimentos garantem que quaisquer alterações sejam adequadamente avaliadas, aprovadas e documentadas para manter a conformidade regulatória e a qualidade do produto.
Normas de Documentação e Rastreabilidade
As tecnologias farmacêuticas de separação exigem sistemas abrangentes de documentação que acompanhem o desempenho dos equipamentos, as atividades de manutenção e os parâmetros do processo ao longo do ciclo de vida do produto. Esses registros devem ser mantidos em conformidade com os requisitos regulatórios e disponibilizados para inspeção pelas autoridades reguladoras.
Os requisitos de rastreabilidade para as tecnologias farmacêuticas de separação incluem a manutenção de registros detalhados dos materiais de alimentação, das condições de processamento e das saídas do produto para cada lote de produção. Essas informações permitem uma investigação rápida de problemas de qualidade e apoiam os procedimentos de recolhimento do produto, se necessário.
Os sistemas eletrônicos de registro utilizados com as tecnologias farmacêuticas de separação devem cumprir os requisitos regulatórios relativos à integridade dos dados, incluindo disposições para armazenamento seguro, acesso controlado e trilhas de auditoria que registrem todas as modificações ou exclusões de dados ao longo do tempo.
Fatores Econômicos e Operacionais
Investimento de Capital e Custos Operacionais
O custo total de propriedade para tecnologias farmacêuticas de separação inclui a aquisição inicial do equipamento, os custos de instalação, as despesas contínuas com manutenção e o consumo de utilidades ao longo do ciclo de vida do equipamento. Esses custos devem ser avaliados em comparação com os volumes de produção esperados e as margens do produto para determinar a viabilidade econômica.
Os custos operacionais para tecnologias farmacêuticas de separação abrangem consumíveis, consumo de energia, requisitos de mão de obra e despesas com descarte de resíduos. Sistemas de separação energeticamente eficientes podem proporcionar economias significativas ao longo da vida útil do equipamento, especialmente em operações de alta produtividade, nas quais os custos com utilidades representam uma parcela substancial das despesas operacionais.
Os custos de manutenção das tecnologias farmacêuticas de separação variam significativamente conforme a complexidade dos equipamentos, o ambiente operacional e os requisitos de manutenção. Sistemas mecânicos simples de separação normalmente apresentam custos de manutenção mais baixos em comparação com sistemas complexos de separação cromatográfica ou química, que exigem suporte técnico especializado e componentes de reposição.
Ciclo de Vida da Tecnologia e Risco de Obsolescência
A vida útil esperada das tecnologias farmacêuticas de separação deve ser avaliada em relação ao ciclo de vida previsto do produto e ao ambiente regulatório. Tecnologias com longa vida útil e suporte consolidado de fornecedores oferecem maior valor a longo prazo e reduzem o risco de obsolescência durante períodos críticos de produção.
A estabilidade do fornecedor e a disponibilidade de suporte técnico são fatores cruciais na seleção de tecnologias farmacêuticas de separação, pois os fabricantes de equipamentos devem oferecer suporte contínuo para peças de reposição, assistência técnica e atualizações relativas à conformidade regulatória ao longo do ciclo de vida do equipamento.
As vias de atualização tecnológica devem ser consideradas ao implementar tecnologias farmacêuticas de separação, para garantir que os equipamentos possam ser modificados ou aprimorados à medida que os requisitos de produção evoluem ou novos requisitos regulatórios entram em vigor, sem a necessidade de substituição completa.
Estratégias de Implementação e Otimização
Integração com Sistemas de Manufatura Existentes
A implementação bem-sucedida de tecnologias farmacêuticas de separação exige uma integração cuidadosa com a infraestrutura de fabricação existente, incluindo processos a montante e a jusante, sistemas de utilidades e sistemas de controle. Essa integração assegura o fluxo contínuo de materiais e a eficiência global ideal do processo, mantendo simultaneamente os padrões de qualidade do produto.
A compatibilidade do sistema de controle é essencial ao integrar tecnologias farmacêuticas de separação com equipamentos de fabricação já existentes. Os sistemas modernos de separação devem oferecer protocolos de comunicação padronizados e interfaces de dados que permitam a integração perfeita com os sistemas de controle e monitoramento de toda a planta.
Os requisitos de treinamento dos operadores para tecnologias farmacêuticas de separação devem ser avaliados para garantir que haja expertise adequada disponível para a operação segura e eficaz dos equipamentos. Os programas de treinamento devem abranger a operação normal, a resolução de problemas, os procedimentos de manutenção e os protocolos de resposta a emergências específicos à tecnologia de separação selecionada.
Monitoramento e Otimização de Desempenho
Sistemas de monitoramento contínuo para tecnologias farmacêuticas de separação permitem a avaliação em tempo real do desempenho da separação e a detecção precoce de possíveis problemas que possam afetar a qualidade do produto. Esses sistemas devem acompanhar indicadores-chave de desempenho, como eficiência de separação, taxas de produtividade e parâmetros de qualidade do produto.
A otimização de processos para tecnologias farmacêuticas de separação envolve a avaliação sistemática dos parâmetros operacionais para maximizar o desempenho da separação, minimizando ao mesmo tempo os custos operacionais e mantendo a conformidade regulatória. Essa otimização deve basear-se em experimentos estatisticamente planejados e em métodos analíticos validados.
As avaliações regulares de desempenho para tecnologias farmacêuticas de separação ajudam a identificar oportunidades de melhoria e garantem a conformidade contínua com os requisitos regulatórios em constante evolução. Essas avaliações devem incluir a análise de dados do processo, registros de manutenção e tendências de qualidade do produto, a fim de apoiar iniciativas de melhoria contínua.
Perguntas Frequentes
Quais são os fatores mais críticos na escolha de tecnologias farmacêuticas de separação?
Os fatores mais críticos incluem os requisitos de conformidade regulatória, as especificações de pureza do produto, a escala de produção e o custo total de propriedade. A tecnologia selecionada deve atender aos padrões de Boas Práticas de Fabricação, ao mesmo tempo em que alcança a eficiência de separação exigida e mantém a viabilidade econômica para os volumes de produção pretendidos.
Como os requisitos regulatórios influenciam a seleção de tecnologias farmacêuticas de separação?
Os requisitos regulatórios determinam que as tecnologias farmacêuticas de separação devem estar em conformidade com as diretrizes de Boas Práticas de Fabricação, incluindo a validação de equipamentos, sistemas de documentação e procedimentos de controle de alterações. Esses requisitos frequentemente favorecem tecnologias consolidadas, com aceitação regulatória comprovada e suporte abrangente dos fornecedores para atividades de validação.
Qual é o cronograma típico de validação para a implementação de novas tecnologias farmacêuticas de separação?
Os prazos para validação de tecnologias farmacêuticas de separação normalmente variam de 6 a 18 meses, dependendo da complexidade do equipamento e dos requisitos regulatórios. Esse cronograma inclui as fases de qualificação de instalação, qualificação operacional, qualificação de desempenho e validação de processo, que devem ser concluídas antes da produção comercial.
Como você avalia a viabilidade a longo prazo das tecnologias farmacêuticas de separação?
A avaliação da viabilidade a longo prazo leva em consideração a maturidade da tecnologia, a estabilidade do fornecedor, os requisitos de manutenção e a aceitação regulatória. Tecnologias com histórico consolidado, suporte confiável dos fornecedores e compatibilidade com as tendências regulatórias emergentes oferecem maior valor a longo prazo e reduzem o risco de obsolescência nas operações de fabricação farmacêutica.
Sumário
- Compreensão das Categorias de Tecnologias de Separação Farmacêutica
- Avaliação dos Requisitos e Especificações do Processo
- Considerações Regulatórias e de Conformidade
- Fatores Econômicos e Operacionais
- Estratégias de Implementação e Otimização
-
Perguntas Frequentes
- Quais são os fatores mais críticos na escolha de tecnologias farmacêuticas de separação?
- Como os requisitos regulatórios influenciam a seleção de tecnologias farmacêuticas de separação?
- Qual é o cronograma típico de validação para a implementação de novas tecnologias farmacêuticas de separação?
- Como você avalia a viabilidade a longo prazo das tecnologias farmacêuticas de separação?