La selección de las tecnologías farmacéuticas de separación adecuadas es una decisión crítica que afecta directamente la calidad del producto, el cumplimiento normativo y la eficiencia operativa en la fabricación farmacéutica. Esta elección implica evaluar múltiples factores, entre ellos los compuestos específicos que se están procesando, los niveles de pureza requeridos, los volúmenes de producción y los requisitos normativos que rigen los procesos de fabricación farmacéutica.

La industria farmacéutica depende de métodos de separación precisos para garantizar que los principios activos farmacéuticos cumplan rigurosos estándares de calidad, manteniendo al mismo tiempo la rentabilidad y la escalabilidad. Comprender el marco de decisión para las tecnologías de separación farmacéutica permite a los fabricantes optimizar sus procesos, reducir los riesgos de contaminación y lograr especificaciones de producto consistentes que satisfagan tanto los requisitos de aprobación regulatoria como los de viabilidad comercial.
Comprensión de las categorías de tecnología de separación farmacéutica
Tecnologías de Separación Mecánica
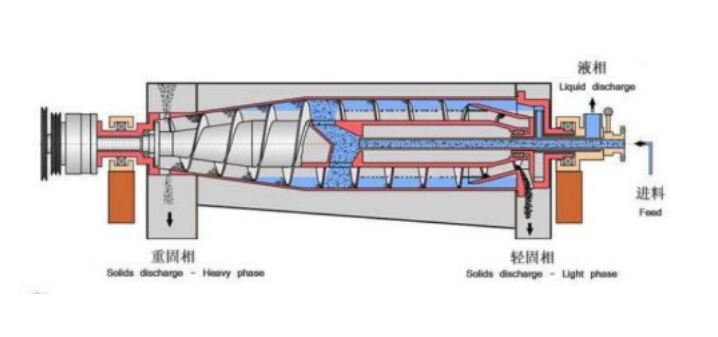
Las tecnologías mecánicas de separación farmacéutica utilizan fuerzas físicas para separar partículas en función de diferencias de tamaño, densidad o forma. Estos métodos incluyen la centrifugación, la filtración y los procesos de tamizado, que operan sin reacciones químicas ni cambios de fase. Los separadores centrífugos, especialmente las centrífugas decantadoras, destacan por su capacidad para separar partículas sólidas de fases líquidas en la fabricación farmacéutica.
La selección de tecnologías mecánicas de separación farmacéutica depende de la distribución del tamaño de partícula, las diferencias de densidad entre fases y la eficiencia de separación requerida. Estos sistemas ofrecen ventajas en términos de operación continua, escalabilidad y contaminación química mínima, lo que los hace adecuados para el procesamiento de intermedios farmacéuticos y productos finales, donde mantener la integridad química es fundamental.
Los métodos mecánicos de separación también proporcionan un excelente control sobre parámetros operativos como la fuerza centrífuga (G-force), el tiempo de residencia y las tasas de caudal. Este control permite a los fabricantes farmacéuticos optimizar el rendimiento de la separación, al tiempo que mantienen una calidad de producto constante y cumplen con los requisitos reglamentarios aplicables al equipo de procesamiento farmacéutico.
Métodos químicos y cromatográficos de separación
Los enfoques de separación química en las tecnologías farmacéuticas de separación implican procesos selectivos de disolución, precipitación o extracción que aprovechan las diferencias en las propiedades químicas entre los compuestos objetivo y las impurezas. Estos métodos suelen ofrecer una mayor selectividad que los enfoques mecánicos, pero requieren una consideración cuidadosa de la compatibilidad química y de los requisitos de procesamiento posterior.
Las tecnologías farmacéuticas de separación cromatográfica ofrecen una precisión excepcional para la purificación de principios activos farmacéuticos y la eliminación de impurezas estrechamente relacionadas. Estos sistemas utilizan fases estacionarias y móviles para lograr una separación selectiva basada en interacciones moleculares, aunque normalmente operan en modo discontinuo y requieren experiencia especializada para su optimización y mantenimiento.
La elección entre métodos químicos y cromatográficos depende de los niveles de pureza requeridos, la escala de operación y las consideraciones económicas. Aunque estas tecnologías farmacéuticas de separación pueden lograr una selectividad muy elevada, suelen implicar costos operativos más altos y un control de proceso más complejo en comparación con los enfoques mecánicos de separación.
Evaluación de los requisitos y especificaciones del proceso
Normas de calidad y pureza del producto
Las tecnologías farmacéuticas de separación deben seleccionarse en función de los requisitos específicos de pureza establecidos por las normas farmacopeicas y las autoridades reguladoras. El nivel de pureza objetivo influye directamente en la complejidad y el costo del sistema de separación, ya que unos requisitos de pureza más elevados suelen exigir múltiples etapas de separación o tecnologías más sofisticadas.
Comprender la naturaleza y la concentración de las impurezas presentes en el material de alimentación es fundamental para seleccionar las tecnologías farmacéuticas adecuadas de separación. Algunas impurezas pueden requerir mecanismos específicos de separación, mientras que otras pueden eliminarse eficazmente mediante equipos de separación de propósito general, como centrífugas de alta eficiencia o sistemas avanzados de filtración.
También debe tenerse en cuenta, al seleccionar tecnologías farmacéuticas de separación, los métodos analíticos utilizados para verificar el rendimiento de la separación. El sistema de separación elegido debe producir productos que puedan analizarse fácilmente mediante los métodos estándar de ensayo farmacéutico, cumpliendo al mismo tiempo las especificaciones establecidas en cuanto a identidad, pureza y potencia.
Escala de producción y requisitos de caudal
Los requisitos de volumen de producción influyen significativamente en la selección de las tecnologías farmacéuticas de separación, ya que distintas tecnologías presentan características variables de escalabilidad y capacidades de caudal. Las separaciones a pequeña escala en laboratorio pueden utilizar enfoques diferentes a los empleados en la producción comercial a gran escala, lo que exige una consideración cuidadosa de la viabilidad de la escalación.
Las preferencias entre operación continua y por lotes también afectan la elección de las tecnologías farmacéuticas de separación. Los sistemas de separación continua, como tecnologías de separación farmacéutica los que utilizan centrífugas decantadoras, ofrecen ventajas para la producción a alto volumen, mientras que los sistemas por lotes pueden proporcionar un mejor control para productos especializados o de alto valor.
La flexibilidad para manejar composiciones variables de la alimentación y horarios de producción debe evaluarse al seleccionar tecnologías farmacéuticas de separación. Los sistemas que pueden adaptarse a cambios en las características de la alimentación o en las demandas de producción ofrecen ventajas operativas y contribuyen a optimizar la eficiencia general de la fabricación.
Consideraciones regulatorias y de cumplimiento
Requisitos de Buenas Prácticas de Fabricación
Todas las tecnologías farmacéuticas de separación deben cumplir con las directrices de Buenas Prácticas de Manufactura que regulan el diseño, la operación y el mantenimiento de los equipos en las instalaciones farmacéuticas. Estos requisitos incluyen especificaciones sobre los materiales de construcción, los acabados superficiales, los procedimientos de limpieza y los sistemas de documentación que garantizan la calidad del producto y la seguridad del paciente.
Los requisitos de validación para las tecnologías farmacéuticas de separación implican ensayos y documentación exhaustivos para demostrar que el equipo produce sistemáticamente productos que cumplen con las especificaciones predeterminadas. Este proceso incluye las fases de calificación de instalación, calificación operacional y calificación de rendimiento, que deben completarse antes de la puesta en marcha comercial.
Se deben establecer procedimientos de control de cambios para las tecnologías farmacéuticas de separación con el fin de gestionar las modificaciones de los parámetros operativos, los procedimientos de mantenimiento o las configuraciones del equipo. Estos procedimientos garantizan que cualquier cambio sea evaluado, aprobado y documentado adecuadamente para mantener el cumplimiento normativo y la calidad del producto.
Normas de Documentación y Trazabilidad
Las tecnologías farmacéuticas de separación requieren sistemas integrales de documentación que registren el rendimiento de los equipos, las actividades de mantenimiento y los parámetros del proceso a lo largo del ciclo de vida del producto. Estos registros deben conservarse conforme a los requisitos reglamentarios y estar disponibles para su inspección por parte de las autoridades reguladoras.
Los requisitos de trazabilidad para las tecnologías farmacéuticas de separación incluyen la conservación de registros detallados de los materiales de alimentación, las condiciones de procesamiento y los productos obtenidos en cada lote de producción. Esta información permite una investigación rápida de los problemas de calidad y respalda los procedimientos de retirada del producto, si fuera necesario.
Los sistemas electrónicos de registro utilizados con las tecnologías farmacéuticas de separación deben cumplir con los requisitos reglamentarios sobre integridad de los datos, incluidas las disposiciones relativas al almacenamiento seguro, el acceso controlado y las pistas de auditoría que registren todas las modificaciones o eliminaciones de los datos a lo largo del tiempo.
Factores Económicos y Operativos
Inversión de Capital y Costos Operativos
El costo total de propiedad de las tecnologías farmacéuticas de separación incluye la compra inicial del equipo, los costos de instalación, los gastos continuos de mantenimiento y el consumo de servicios auxiliares durante todo el ciclo de vida del equipo. Estos costos deben evaluarse en relación con los volúmenes de producción previstos y los márgenes del producto para determinar su viabilidad económica.
Los costos operativos de las tecnologías farmacéuticas de separación comprenden los consumibles, el consumo energético, los requisitos de mano de obra y los gastos de eliminación de residuos. Los sistemas de separación eficientes desde el punto de vista energético pueden generar importantes ahorros de costos a lo largo de la vida útil del equipo, especialmente en operaciones de alto rendimiento, donde los costos de los servicios auxiliares representan una parte sustancial de los gastos operativos.
Los costos de mantenimiento de las tecnologías farmacéuticas de separación varían significativamente según la complejidad del equipo, el entorno operativo y los requisitos de mantenimiento. Los sistemas mecánicos simples de separación suelen tener costos de mantenimiento más bajos en comparación con los sistemas complejos de separación cromatográfica o química, que requieren soporte técnico especializado y componentes de reemplazo.
Ciclo de vida de la tecnología y riesgo de obsolescencia
La vida útil prevista de las tecnologías farmacéuticas de separación debe evaluarse en función del ciclo de vida esperado del producto y del entorno regulatorio. Las tecnologías con una larga vida útil y un soporte establecido por parte de los proveedores ofrecen un mayor valor a largo plazo y reducen el riesgo de obsolescencia durante períodos críticos de producción.
La estabilidad del proveedor y la disponibilidad de soporte técnico son factores cruciales al seleccionar tecnologías farmacéuticas de separación, ya que los fabricantes de equipos deben ofrecer soporte continuo para piezas de repuesto, asistencia técnica y actualizaciones sobre el cumplimiento normativo durante todo el ciclo de vida del equipo.
Al implementar tecnologías farmacéuticas de separación, deben considerarse las vías de actualización tecnológica para garantizar que los equipos puedan modificarse o mejorarse conforme evolucionen los requisitos de producción o se apliquen nuevos requisitos normativos, sin necesidad de sustituirlos por completo.
Estrategias de Implementación y Optimización
Integración con sistemas de fabricación existentes
La implementación exitosa de tecnologías farmacéuticas de separación requiere una integración cuidadosa con la infraestructura de fabricación existente, incluidos los procesos aguas arriba y aguas abajo, los sistemas auxiliares y los sistemas de control. Esta integración asegura un flujo de materiales fluido y una eficiencia general óptima, manteniendo al mismo tiempo los estándares de calidad del producto.
La compatibilidad del sistema de control es esencial al integrar tecnologías farmacéuticas de separación con los equipos de fabricación existentes. Los sistemas modernos de separación deben ofrecer protocolos de comunicación estandarizados e interfaces de datos que permitan una integración perfecta con los sistemas de control y supervisión a escala de planta.
Los requisitos de formación para los operadores de tecnologías farmacéuticas de separación deben evaluarse para garantizar la disponibilidad de la experiencia adecuada en la operación segura y eficaz del equipo. Los programas de formación deben abarcar la operación normal, la resolución de incidencias, los procedimientos de mantenimiento y los protocolos de respuesta ante emergencias específicos de la tecnología de separación seleccionada.
Monitoreo y Optimización del Rendimiento
Los sistemas de monitorización continua para tecnologías farmacéuticas de separación permiten la evaluación en tiempo real del rendimiento de la separación y la detección temprana de posibles problemas que podrían afectar a la calidad del producto. Estos sistemas deben registrar indicadores clave de rendimiento, como la eficiencia de separación, las tasas de producción y los parámetros de calidad del producto.
La optimización de procesos para tecnologías farmacéuticas de separación implica la evaluación sistemática de los parámetros operativos para maximizar el rendimiento de la separación, minimizando al mismo tiempo los costos operativos y manteniendo el cumplimiento normativo.
Las revisiones periódicas del rendimiento de las tecnologías farmacéuticas de separación ayudan a identificar oportunidades de mejora y garantizan el cumplimiento continuo de los requisitos normativos en constante evolución. Estas revisiones deben incluir el análisis de datos del proceso, registros de mantenimiento y tendencias de calidad del producto para respaldar las iniciativas de mejora continua.
Preguntas frecuentes
¿Cuáles son los factores más críticos al seleccionar tecnologías farmacéuticas de separación?
Los factores más críticos incluyen los requisitos de cumplimiento normativo, las especificaciones de pureza del producto, la escala de producción y el costo total de propiedad. La tecnología seleccionada debe cumplir con las normas de Buenas Prácticas de Manufactura, lograr la eficiencia de separación requerida y mantener su viabilidad económica para los volúmenes de producción previstos.
¿Cómo influyen los requisitos normativos en la selección de tecnologías farmacéuticas de separación?
Los requisitos normativos exigen que las tecnologías farmacéuticas de separación cumplan con las directrices de Buenas Prácticas de Manufactura, incluidas la validación de equipos, los sistemas de documentación y los procedimientos de control de cambios. Estos requisitos suelen favorecer tecnologías consolidadas con una aceptación normativa comprobada y un soporte integral por parte del proveedor para las actividades de validación.
¿Cuál es el plazo típico de validación para la implementación de nuevas tecnologías farmacéuticas de separación?
Los plazos de validación para las tecnologías farmacéuticas de separación suelen oscilar entre 6 y 18 meses, según la complejidad del equipo y los requisitos regulatorios. Este plazo incluye las fases de cualificación de instalación, cualificación operativa, cualificación de rendimiento y validación del proceso, que deben completarse antes de la producción comercial.
¿Cómo evalúa la viabilidad a largo plazo de las tecnologías farmacéuticas de separación?
La evaluación de la viabilidad a largo plazo tiene en cuenta la madurez tecnológica, la estabilidad del proveedor, los requisitos de mantenimiento y la aceptación regulatoria. Las tecnologías con antecedentes consolidados, soporte fiable por parte del proveedor y compatibilidad con las tendencias regulatorias emergentes ofrecen un mayor valor a largo plazo y reducen el riesgo de obsolescencia en las operaciones de fabricación farmacéutica.
Tabla de contenidos
- Comprensión de las categorías de tecnología de separación farmacéutica
- Evaluación de los requisitos y especificaciones del proceso
- Consideraciones regulatorias y de cumplimiento
- Factores Económicos y Operativos
- Estrategias de Implementación y Optimización
-
Preguntas frecuentes
- ¿Cuáles son los factores más críticos al seleccionar tecnologías farmacéuticas de separación?
- ¿Cómo influyen los requisitos normativos en la selección de tecnologías farmacéuticas de separación?
- ¿Cuál es el plazo típico de validación para la implementación de nuevas tecnologías farmacéuticas de separación?
- ¿Cómo evalúa la viabilidad a largo plazo de las tecnologías farmacéuticas de separación?